-安心・信頼のデータをタイムリーに!-
- 初期探索研究(ヒット化合物の安全性プロファイリング)、リード化合物の最適化過程を推進する各種 in vitro 安全性試験メニューをそろえています。
- WEBシステムにより依頼から結果報告まで、ハイスループットADMEスクリーニングと連繋して信頼性あるデータを迅速に提供します。
- プロジェクト、化合物の特性及び課題に応じて、お客様のニーズに合わせた最適な安全性評価戦略をご提案します。
Axceleadのin vitro安全性スクリーニング
豊富なメニューから、お客様のニーズに合わせた最適なソリューションをご提案します。
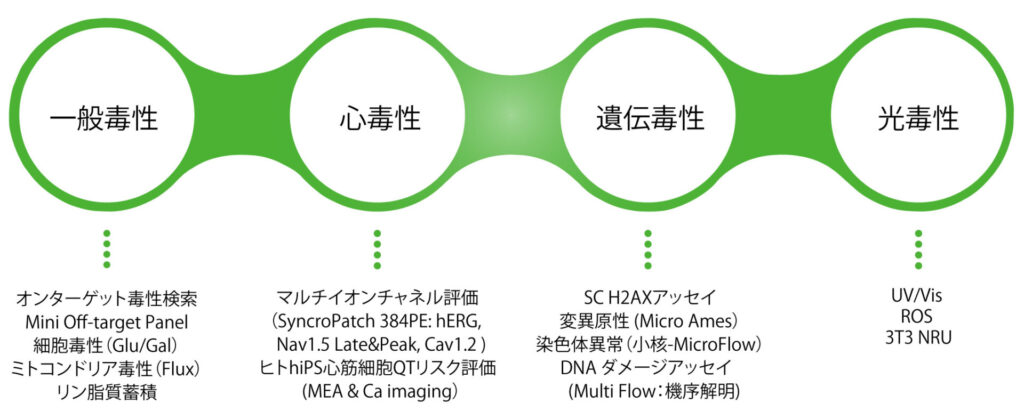
Axceleadが提供する注目のアッセイ
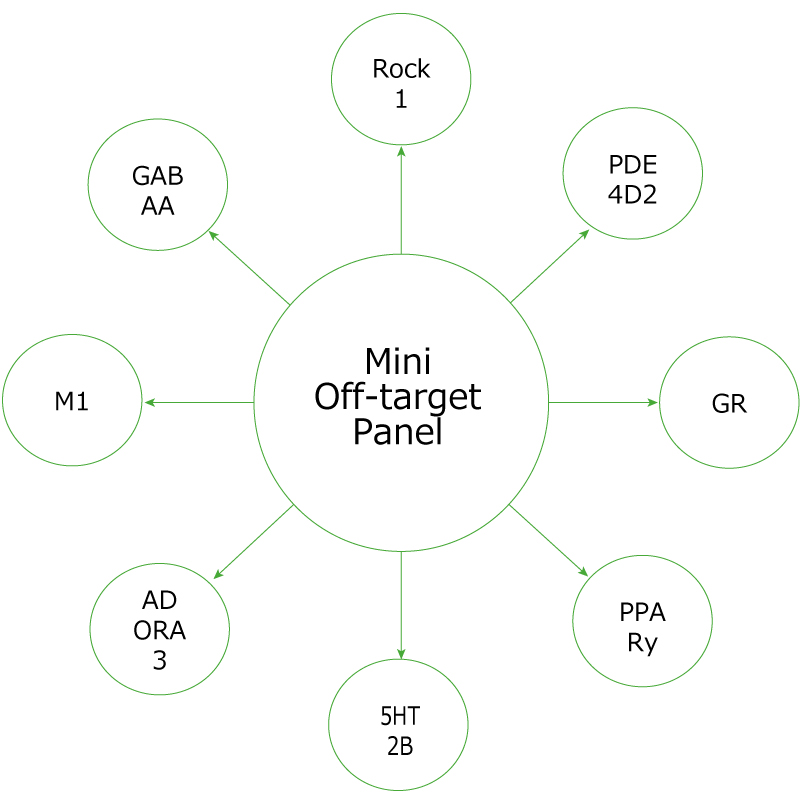
Off-Target 毒性誘発リスク予測 (Mini Off-target Panel)
厳選した8標的で効率的に被験物質の Off-Target 毒性発現を予測します
複数のターゲットに無差別に結合する化合物は、予期しない薬理活性を引き起こし、有害作用につな
がる可能性があります。初期の研究段階でそのような化合物を避けることにより、臨床成功確率の高い
化合物の特定に貢献します。
Axcelead が行うMini Off-target Panel の3 つの強み
- 多様性: 様々な Gene family から被験物質がヒットしやすい8標的を選抜。一般的なGPCR をメインとした大規模パネルよりも効率的に被験物質のOff-Target 毒性発現を予測します。
- 豊富な測定実績: 年間1000 化合物以上の測定実績。
in vivo で何らかの副作用を誘発し易くなるといわれる2 ターゲット以上のヒット率は16.3%(2023 年度実績) です。 - ハイスループット: 毎週アッセイを実施可能。
アッセイ開始から約1 週間で結果を報告しますので、効率的にOff-Target 回避策を次の合成展開に反映できます。
Screening γH2AX assay (SC H2AX)
初期遺伝毒性評価を組み込むことで、予期せぬ小核陽性による開発断念を低減できます
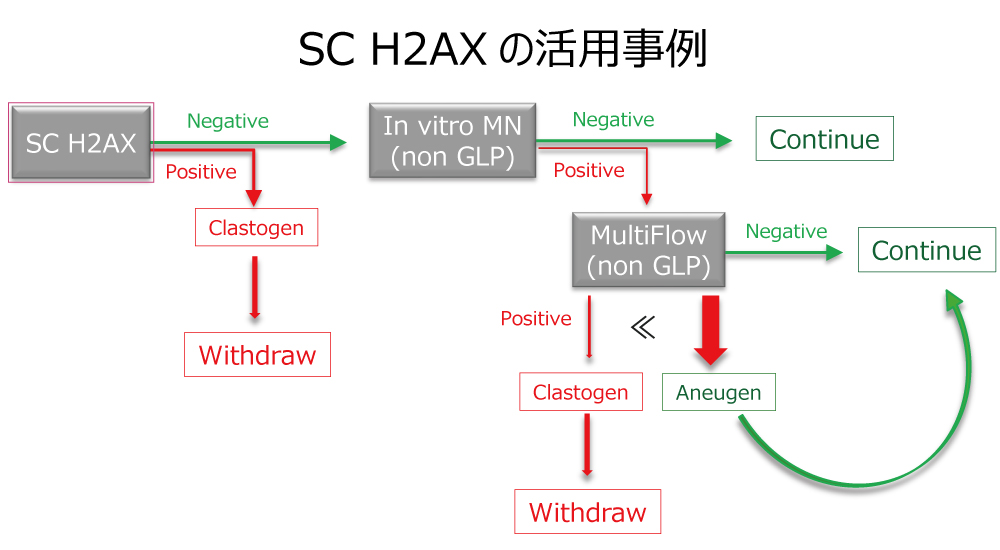
γH2AX はDNA2 本鎖切断に伴い誘導されることから、染色体構造異常誘発物質 (Clastogen) の
予測マーカーとして利用されています。
Axcelead のSC H2AX 試験では、フローサイトメーターを用いて化合物によるγH2AX 誘導を評価しま
す。0.15mg 程度の極少量のサンプルかつ短期(5 日間) のTAT*1 のためLG/LO2*2 ステージ評価に
最適です。
*1 : Tern Around Time、CARS システム上での案件受付~報告までの最短営業日数となります。
*2: Lead Generation / Optimization
一般毒性試験(細胞毒性、ミトコンドリア毒性、リン脂質蓄積、Promiscuity)
医薬品候補化合物のステージや安全性懸念状況に合わせて、スループットの高い評価からリスク回避をサポートする機序解明評価に対応します。
■細胞毒性試験:HepG2細胞を用いたin vitro細胞毒性試験により、in vivoにおいて標的臓器毒性誘発懸念の小さい化合物選抜をサポートします。毎週120(24/72hr cytotox)あるいは320(24hr cytotox)化合物の評価能力があります。
- Cytotox Glu/Gal(24hr)試験:3 濃度で短期曝露下における細胞生存率(ATPを指標)を算出するハイスループット試験
- Cytotox Glu/Gal(24hr)+ Glu(72hr)試験:8 濃度で短期・長期暴露下における細胞生存率(ATPを指標)及びIC50値を算出する精査試験
高濃度グルコース(Glu)あるいは高濃度ガラクトース(Gal)培地で馴化した2種類のHepG2 細胞を使用/比較(Glu IC50/Gal IC50 比)することで、薬物性肝障害を初めとする臓器毒性との関連性が指摘されるミトコンドリア障害も評価できます。
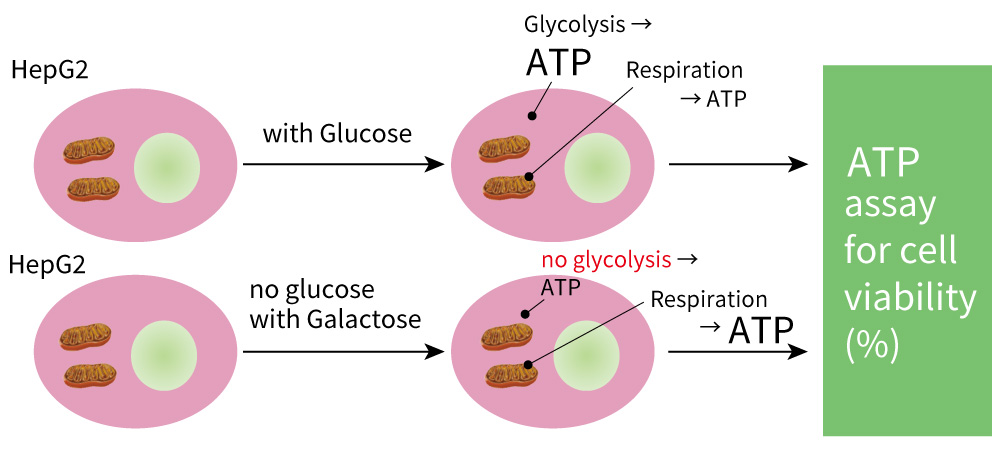
■ミトコンドリア毒性試験(Flux Analyzer(Flux analyzer XF96e)法、HepG2細胞): 4 濃度でのミトコンドリア呼吸による酸素消費速度(OCR)と解糖による細胞外酸性化度(ECAR)を評価します。一般的に、上述のCytotox Glu/Gal assayよりも感度良くミトコンドリア毒性を検出でき、その抑制機序も検討することができます。
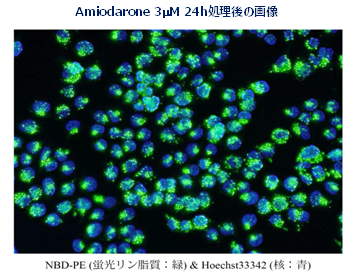
■Phospholipidosis 試験(HepG2 細胞): 4 濃度でのNBD-PE蓄積量(AUC)を算出し、陽性対照薬 amiodarone のAUCと比較することで、リン脂質蓄積作用を評価します。
■Promiscuity 8 panel 試験:蛍光又は RI 標識したリガンドを用いた小規模受容体結合試験。毒性学的懸念につながる標的(Off-Targets)の検出ではなく、様々なGene familyから被験物質がヒットしやすい標的を選抜することで、GPCRをメインとした大規模パネルよりも効率的に被験物質のPromiscuity特性(Off-Target 毒性の発現のしやすさ)を予測します。
心毒性(QTリスク/催不整脈リスク)試験
医薬品候補化合物のステージに合わせて、スループットの高い自動バッチクランプ法によるチャネル電流評価からhiPS心筋細胞を用いたQTリスク(QT延長/催不整脈)評価に対応します。
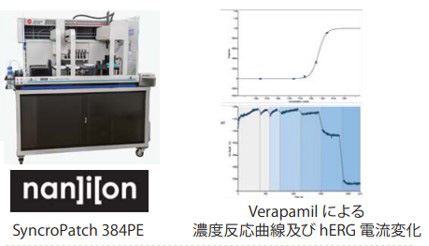
■心臓マルチイオンチャネル電流試験 (SyncroPatch 384PE*):
各チャネルを安定高発現させたCHOあるいはHEK細胞を用い、各チャネルを流れる電流(1.hERG, 2. Nav1.5 Peak, 3. Nav1.5 Late & Peak, 4. Cav1.2)に及ぼす影響を Auto-mated patch clamp法で評価します。
- 384 well plate を用いたハイスループット評価系
- 細胞解凍当日中に実験(長期休暇後も速やかに評価可能)
- Manual patch clamp法と良好な相関
- 吸着性の高い化合物にも対応(ガラスコート plate使用)
- 4 濃度の累積投与評価 (hERGのみ)でwell間差を最小に、評価能力を拡充
- 提供データ : IC50、Hill 係数、各濃度の阻害率、(陽性対照物質の評価結果**)
*: Nanion Technologies GmbHの商標または登録商標です。
**: hERG電流に及ぼす陽性対照物質(verapamil)の作用曲線

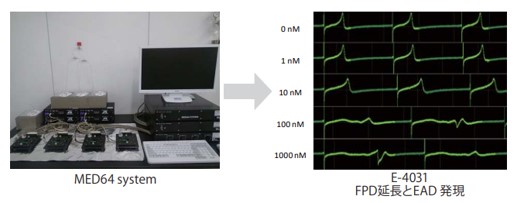
■心筋細胞を用いたQTリスク(QT延長/催不整脈)試験:ヒトiPS細胞由来心筋細胞を用いた多点微小電極アレイ(MED64 system)あるいは Ca transient 法(FDSS/µCELL)により、FPD(QT)延長及び不整脈誘発リスクを評価します。
遺伝毒性試験
医薬品候補化合物の遺伝毒性スクリーニング・機序解明に対応します。試験組合わせのご提案、結果の解釈や精査要否などのご相談に経験豊富な研究者が対応します。
■探索的 Ames 試験:MicroAmes
24 well寒天プレートを用いる探索的 Ames試験。通常の Ames試験と基本操作はそのままで約 1/15にミニチュア化した試験法です。サルモネラ菌2菌株(TA100株及びTA98株)、代謝活性化及び非代謝活性化の2処理条件下において、突然変異誘発能を評価します。

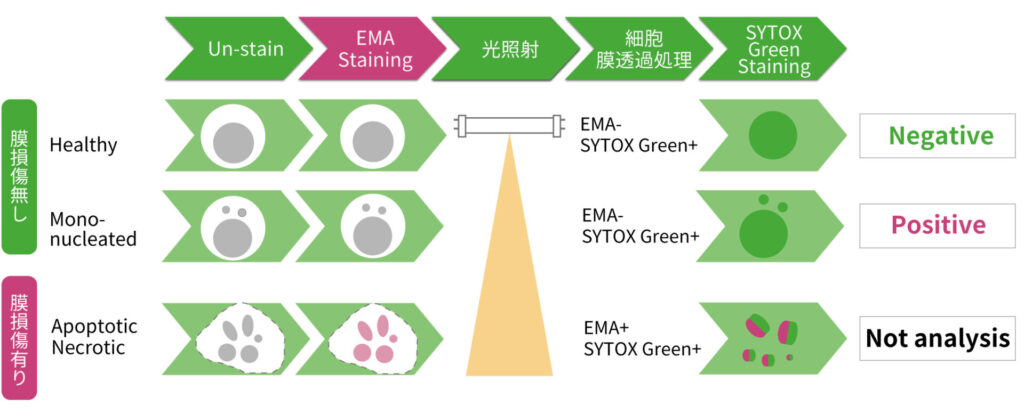
■フローサイトメトリーを用いた探索的 in vitro小核試験: MicroFlow
ヒトリンパ芽球細胞株(TK6 細胞)を用いた探索的な in vitro小核試験。代謝活性化(3 hr)及び非代謝活性化(24 hr)の2処理条件下において、被験物質暴露後の間期細胞に形成された小型の核(小核)をフローサイトメーターで検出することで、染色体異常の誘発を迅速に評価します。
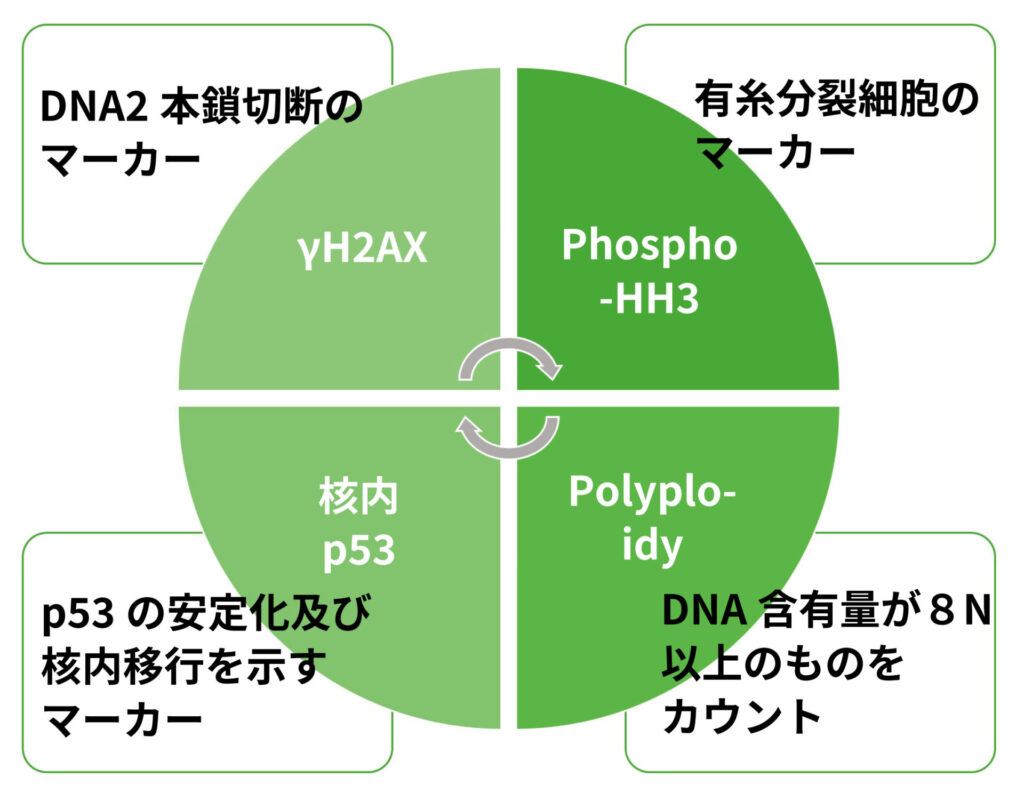
■フローサイトメトリーを用いた in vitro 小核誘発機序解析試験: MultiFlow
ヒトリンパ芽球細胞株(TK6 細胞)を用いた、遺伝毒性発現機序の確認・精査用の試験。代謝活性化(3 hr)及び非代謝活性化(24 hr)の2処理条件下において、DNA二本鎖切断マーカー (γH2AX)、有糸分裂マーカー(pHH3)、核内p53 及び多核細胞(polyploidy)の誘発をフローサイトメーターで評価します。各マーカーの誘導パターンから、染色体構造異常誘発(Clastogen)や異数性誘発(Aneugen)といった、遺伝毒性誘発機序を推察します。
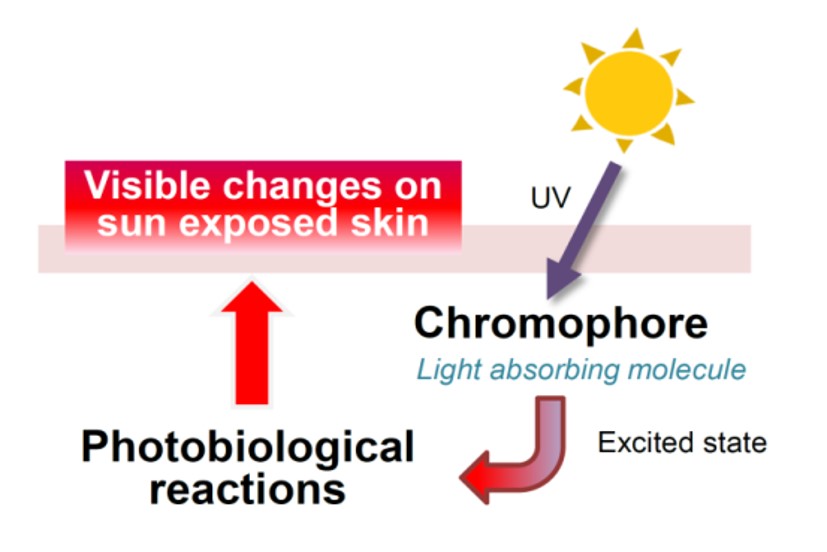
光毒性試験
光毒性は、化学物質と太陽光との相互作用により発生します。Axceleadでは光毒性ポテンシャルを早期に確認するin vitro試験に対応しています。
■紫外/可視光吸収スペクトル試験(UV/Vis)
UV/Visは光毒性の実験的評価要否の基準となる290-700 nmにおけるモル吸光係数(Molar Extinction Coefficient: MEC)を調べる試験。MEC≧1000 L mol-1cm-1の場合、高次の光毒性試験の評価が必要です。使用被験物質量を削減したスクリーニング法も用意しています。
■ROSアッセイ:活性酸素種(ROS: Reactive Oxygen Species)産生試験
被験物質の光化学的特性を指標とした in chemico 法であり、被験物質に擬似太陽光を照射し、singlet oxygen(SO)ならびにsuperoxide anion(SA)の産生を指標として、OECD Test Guideline No.495に準拠した方法により光毒性ポテンシャルを評価します。
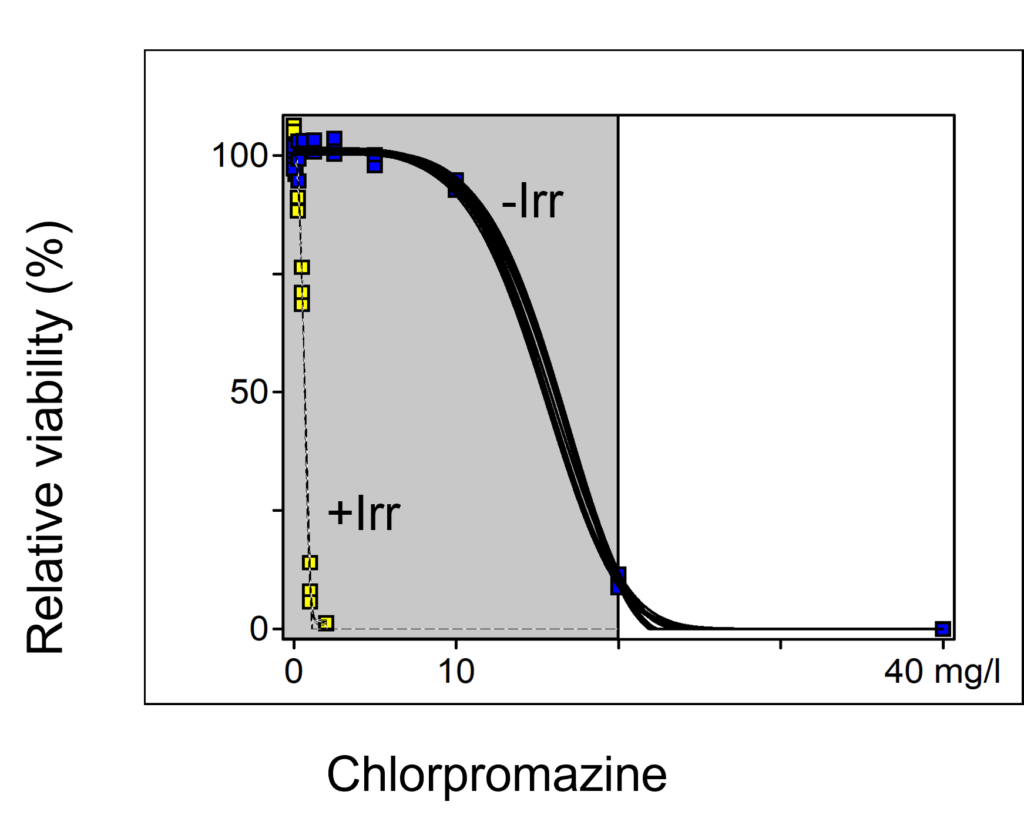
■in vitro光毒性試験:3T3 NRU(Neutral Red Uptake法)
OECD Test Guideline No. 432試験: BALB/c 3T3 細胞を用い、擬似太陽光照射の有無による細胞生存率の差を NRU(Neutral Red Uptake) 法により評価します。
心毒性および光毒性評価については、in vitro screeningから
in vivo 試験までOne team /One stop solutionでトータルサポートします。
■In vivo 心血行動態および心機能試験
大動物(イヌ、サル)を麻酔下あるいは覚醒下無線テレメトリーで、心電図や左心室内圧などの心血行動態や心機能を評価します。また、小動物(ラット)では、覚醒下で心拍数や血圧への影響を、麻酔下では心エコーによる心機能評価を行います。
■In vivo 光毒性試験
定番のヘアレスマウスだけでなく、SDラットやLong-Evansラットにも対応可能。また、GLP試験も受託可能です。経験豊富な研究者が、お客様の目的に応じて最適なモデルをご提案します。