見えれば分かる核酸医薬開発の課題と解決策
近年、核酸医薬品の研究・開発が盛んになり、Lipid Nano Particle (LNP)に内封した核酸の動態・薬効評価、更には効率的に送達させるためのスクリーニング技術開発が進められています。従来、核酸の動態評価や生体内分布の評価には、質量分析による組織抽出物中の核酸定量法が用いられてきました。
しかし、質量分析では、組織中の含有量は検出できますが、位置情報までは確認できません。特に、ターゲット遺伝子のノックダウン活性と定量結果とに乖離がある場合に「組織内分布が確認できれば良いのに!」と思われることはなかったでしょうか?
そのような時にターゲット遺伝子に対するプローブを用いたin situ hybridizationや修飾核酸に特異的に結合する抗体を用いた免疫組織染色で組織内・細胞内での分布を可視化することにより、投与した核酸が狙い通りに標的組織や細胞まで届いたのか、あるいは血管内に蓄積していたのかなど重要な位置情報を知ることができます。
一歩踏み込んだ核酸医薬の動態・薬効評価、
そして毒性MOAについての新たな知見を提供します!
■投与した核酸と、その後を可視化します!
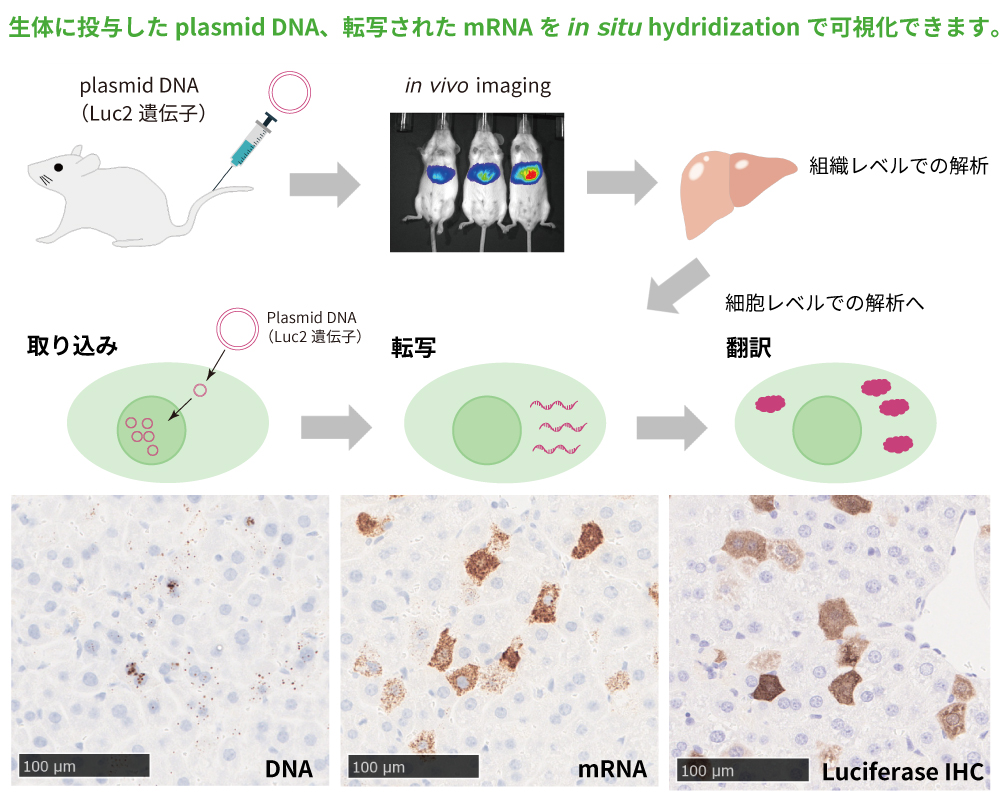
投与したDNA(Plasmid DNA)はターゲット遺伝子に対するプローブを用いたin situ hybridizationで、修飾を施したAntisense oligonucleotide(ASO)の局在は修飾部位に特異的に結合する抗体を用いた免疫組織染色で、細胞レベルでの可視化が可能です。更に、投与した核酸の取り込みをこれらの技術で識別するとともに、転写、翻訳後の産物もin situ hybridizationや免疫組織染色を実施することで、取り込み、転写、翻訳までの一連の流れにおける標的物質を可視化できます。この技術により、一歩踏み込んだ核酸医薬の動態・薬効評価、そして毒性MOAについての新たな知見を提供可能です。
■どんなものでも可視化できるの?
可視化したい核酸の配列に対するプローブをハイブリダイズさせるin situ hybridizationを用いますので、ターゲット遺伝子の配列が分かり、それに対する特異的なプローブを設計/作製できれば可視化が可能です。
■配列が短いASOは?
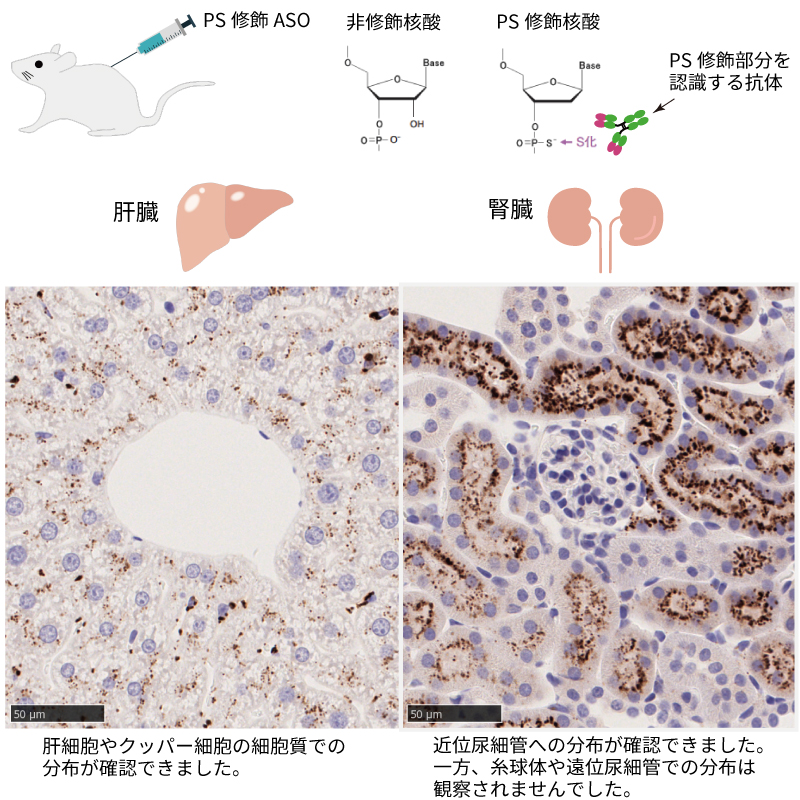
ASOなど配列が短く特異的なプローブの設計が難しい場合でも、Phosphorothioate(PS)修飾されたASOであれば、PS修飾部位に特異的なオリジナル抗体を用いた免疫組織染色により、配列に依存することなく可視化が可能です。
核酸の生体内分布評価をトータルでお引き受けします!
■核酸の局在・質量分析を総合的に評価可能に!
Axceleadでは、可視化技術をもって作製された標本の染色結果から、病理専門家による評価を行うことが可能です。更に、核酸の動態に関する専門部門からのデータも併せ、総合的な評価をご提供することができます。
核酸医薬品の評価に取り組まれている皆様でノックダウン活性と定量結果との乖離など、解釈でお困りの方がいらっしゃいましたら、Axceleadの可視化技術で課題解決に取り組んでみてはいかがでしょうか?是非お声かけください!
◇関連サービスのご紹介◇
