2025/12/11
miRNA解析
-176種類以上のmiRNAを網羅的に解析-
miRNAでバイオマーカー探索しませんか
miRNAとは?
21~23塩基程度の短いノンコーディングRNA(non-coding RNA)で、標的となるメッセンジャーRNA(mRNA)に結合して翻訳抑制を行い、遺伝子を抑制的に制御します。
細胞の分化や個体発生など様々な生命現象に関与し、その発現異常はがんをはじめとする多くの疾患と関係することがわかってきています。
miRNAの特徴は?
- 塩基配列は種を超えて保存されているため、種差の影響を受けにくい
- 臓器特異的なmiRNAが存在する
- 疾患組織と正常組織とでmiRNAプロファイルが異なる
- 血液(血漿・血清)や尿、唾液、脳脊髄液といった様々な体液中にも存在
- 体液中のmiRNAはRNaseの影響を受けにくいため、安定性が高い
miRNA解析
組織採取より低侵襲的で簡便に得られる利点があることから、血液や尿、唾液などの体液中miRNAを用いた疾患マーカーや臓器障害マーカーの探索は加速していくと思われます。Axceleadでは、ヒトで約2,000種類あるといわれているmiRNAのうち、疾患に関連するmiRNAを解析いたします。
miRNA解析から、課題解決に適したバイオマーカーを見つけてみませんか。

少量の検体から網羅的解析が可能です!
200uLの検体からmiRNAを網羅的に解析し、評価します。 たとえ、RNA収量が少なくても、miRNA解析が可能です。
例)健常人由来唾液200 uLからtotal RNAを抽出し、qPCR解析
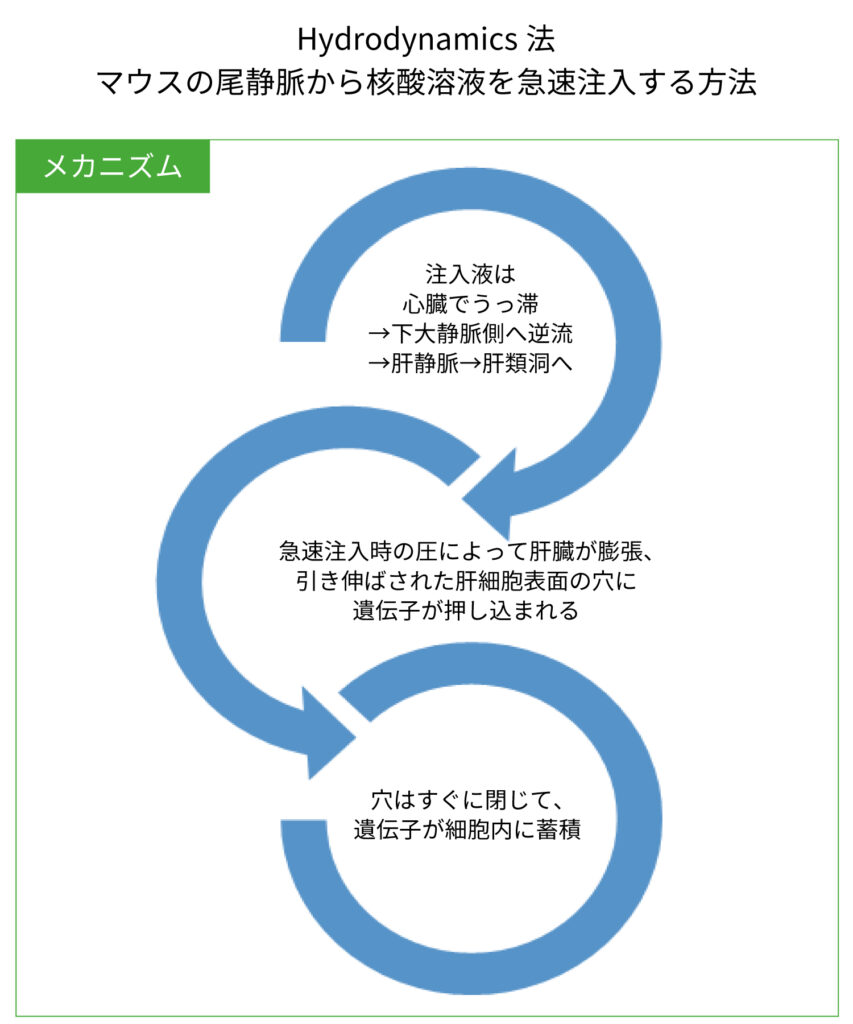
Hydrodynamics法を用いたマウスへのin vivo遺伝子導入
Hydrodynamics法によりマウスへin vivo遺伝子導入することで
動物モデルの可能性を広げます!
- Hydrodynamics法は、遺伝子改変細胞と遺伝子改変動物の中間に位置する、動物を用いて一過性に遺伝子を導入する技術のひとつで、スループット性及び疾患外挿性の両方を兼ね備えた技術です。
- 一過性に遺伝子を導入するその他の方法(LNPやAAV)や遺伝子改変動物と比較して、短期間で簡単に実施できるのが魅力です。
- 主な遺伝子発現臓器は肝臓ですが、血中分泌タンパク(サイトカイン等)も増加させることができます。
- 免疫ヒト化マウスモデルの作製への応用や既存の病態モデルマウスへの追加遺伝子導入も行うことができ、疾患を模倣した多様な動物モデルを短期間で簡単に創出可能なプラットフォームです。
- 肝疾患における創薬ターゲット候補分子のコンセプト検証のサポートに使用することもできます。

迅速で確実な一過性in vivo遺伝子導入
- 導入したい核酸が準備できればすぐに実施可能です(必要に応じてプラスミドDNAの設計/調製もAxceleadにて承ります)。
- 導入に特別な試薬、装置、LNPやAAVのようなキャリア準備は一切不要です。
- 主に肝臓に導入された遺伝子は 数時間後から発現確認可能で、数週間から数カ月間持続します(マウスの系統によります)。
- 適度な回復期間をおけば反復投与することも可能です。
- siRNAやshRNAなどによる遺伝子ノックダウンにも適用可能です。
ヒト遺伝子Knock-In(KI)マウス/ラットを用いた評価をワンストップで実施
ヒト遺伝子KIマウス/ラット(ヒト遺伝子ノックインマウス/ラット、 以下 KIマウス/ラット)は対象となる内在遺伝子にヒト遺伝子を挿入した動物で、種差のある開発化合物の評価や、疾患モデルを作出するために活用されてきました。Axceleadではサルやイヌ、ブタを用いた試験に加え、KIマウス/ラットの作出から薬効・安全性評価、ひいてはIND申請用非臨床試験(薬理、安全性)までワンストップでご提供いたします。

なぜ、今、KIマウス/ラットなのか?
内在のマウス/ラット遺伝子を欠失させてヒト遺伝子と入れ替えて作出するため、種差のある医薬品の評価に有用です。特に、以下のようなケースでKIマウス/ラットを使った評価をお薦めしています。
〈実験用サルの代替動物種として〉
昨今、カニクイザルの価格高騰や輸入制限などによって非臨床試験が実施困難な状況となり、多くの創薬研究プロジェクトが延期や中止に追い込まれていると伺います。
この状況に対し、Axcelead ではヒト遺伝子 KI 動物の活用という選択肢をご提案しております。
本ソリューションについて、詳細のご紹介を希望される方はお問い合わせフォームよりご連絡ください。
〈ニューモダリティ医薬品の評価〉
Off target毒性が発現しにくいと言われているニューモダリティ医薬品の毒性試験では、薬効発現動物を用いてのon target毒性評価が規制当局から求められています。創薬標的をヒト遺伝子に置き換えたKIマウス/ラットを用いた薬理試験において薬効が確認できた場合には、引き続きKIマウス/ラットを用いて毒性試験を実施することで、on target毒性評価が可能となります。
核酸医薬品開発ではエクソン-イントロン構造を保持した長鎖遺伝子配列を発現させたKIマウス/ラットを用いた薬効及び安全性評価が有用になります。特に、Axceleadでは長鎖KIマウスの作出も得意としております。

〈低分子医薬品の評価〉
いずれの動物種を用いても薬効が発現しないケースでは、KIマウス/ラットによって薬効が評価可能となります。また、規制当局からはKIマウス/ラットを用いたon target毒性評価が求められる可能性があります。詳しくはお問い合わせください。
核酸の組織内分布を見る技術
–in situ hybridizationや免疫組織染色を
利用したソリューションー
見えれば分かる核酸医薬開発の課題と解決策
近年、核酸医薬品の研究・開発が盛んになり、Lipid Nano Particle (LNP)に内封した核酸の動態・薬効評価、更には効率的に送達させるためのスクリーニング技術開発が進められています。従来、核酸の動態評価や生体内分布の評価には、質量分析による組織抽出物中の核酸定量法が用いられてきました。
しかし、質量分析では、組織中の含有量は検出できますが、位置情報までは確認できません。特に、ターゲット遺伝子のノックダウン活性と定量結果とに乖離がある場合に「組織内分布が確認できれば良いのに!」と思われることはなかったでしょうか?
そのような時にターゲット遺伝子に対するプローブを用いたin situ hybridizationや修飾核酸に特異的に結合する抗体を用いた免疫組織染色で組織内・細胞内での分布を可視化することにより、投与した核酸が狙い通りに標的組織や細胞まで届いたのか、あるいは血管内に蓄積していたのかなど重要な位置情報を知ることができます。
一歩踏み込んだ核酸医薬の動態・薬効評価、
そして毒性MOAについての新たな知見を提供します!
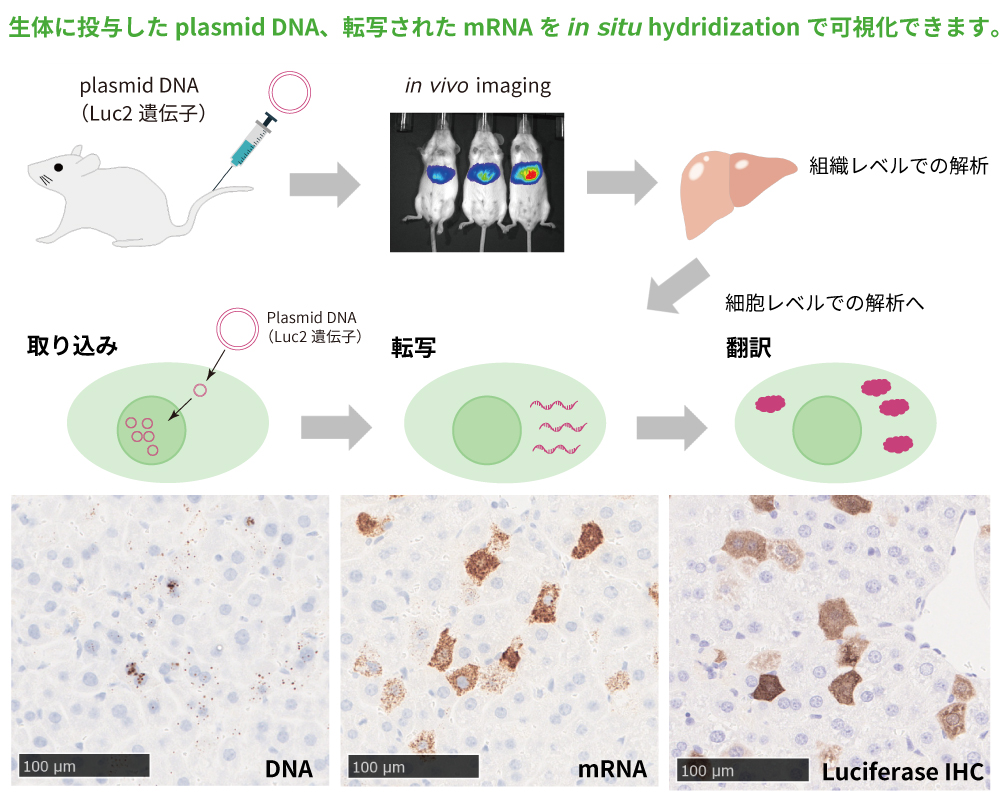
■投与した核酸と、その後を可視化します!
投与したDNA(Plasmid DNA)はターゲット遺伝子に対するプローブを用いたin situ hybridizationで、修飾を施したAntisense oligonucleotide(ASO)の局在は修飾部位に特異的に結合する抗体を用いた免疫組織染色で、細胞レベルでの可視化が可能です。更に、投与した核酸の取り込みをこれらの技術で識別するとともに、転写、翻訳後の産物もin situ hybridizationや免疫組織染色を実施することで、取り込み、転写、翻訳までの一連の流れにおける標的物質を可視化できます。この技術により、一歩踏み込んだ核酸医薬の動態・薬効評価、そして毒性MOAについての新たな知見を提供可能です。
■どんなものでも可視化できるの?
可視化したい核酸の配列に対するプローブをハイブリダイズさせるin situ hybridizationを用いますので、ターゲット遺伝子の配列が分かり、それに対する特異的なプローブを設計/作製できれば可視化が可能です。
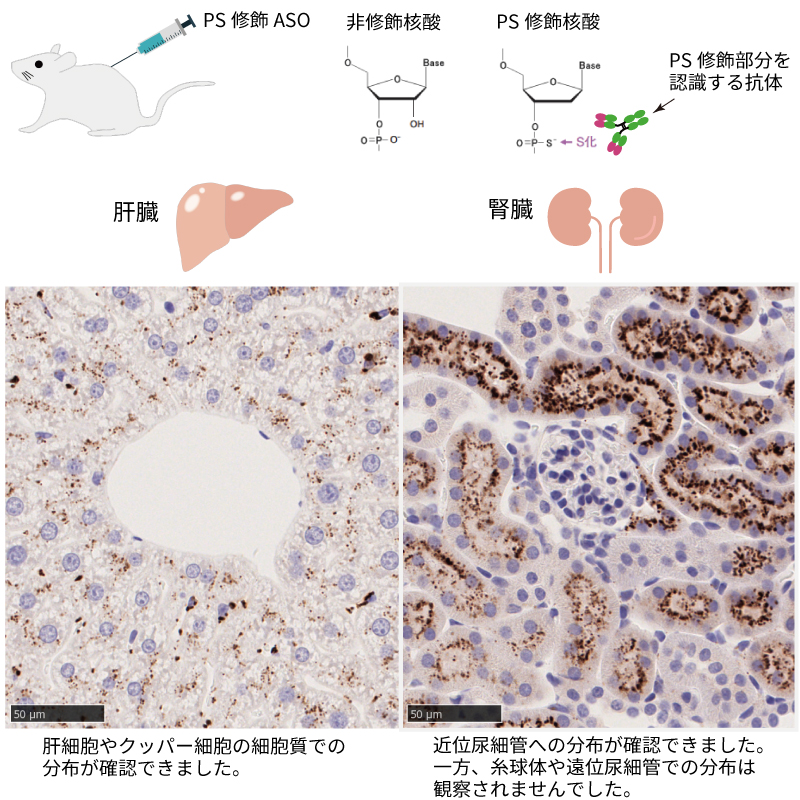
■配列が短いASOは?
ASOなど配列が短く特異的なプローブの設計が難しい場合でも、Phosphorothioate(PS)修飾されたASOであれば、PS修飾部位に特異的なオリジナル抗体を用いた免疫組織染色により、配列に依存することなく可視化が可能です。
核酸の生体内分布評価をトータルでお引き受けします!
■核酸の局在・質量分析を総合的に評価可能に!
Axceleadでは、可視化技術をもって作製された標本の染色結果から、病理専門家による評価を行うことが可能です。更に、核酸の動態に関する専門部門からのデータも併せ、総合的な評価をご提供することができます。
核酸医薬品の評価に取り組まれている皆様でノックダウン活性と定量結果との乖離など、解釈でお困りの方がいらっしゃいましたら、Axceleadの可視化技術で課題解決に取り組んでみてはいかがでしょうか?是非お声かけください!
◇関連サービスのご紹介◇
核酸医薬品オフターゲット効果評価のトータルサービス
核酸医薬品開発の効率化および核酸医薬品開発
プロセス加速化のためのサービスを提供します!
核酸医薬品の開発において、標的以外の配列へのハイブリダイゼーションに起因するオフターゲット効果による毒性は開発の初期段階で回避したい項目の一つです。 Axceleadでは、核酸医薬品候補の多様なオフターゲット効果を予測するために、ヒト肝細胞株を初めとする種々の細胞を用い、ヒトへの外挿性の高いin vitroハイスループットアッセイ系(96および384ウェルフォーマット)を提供します。
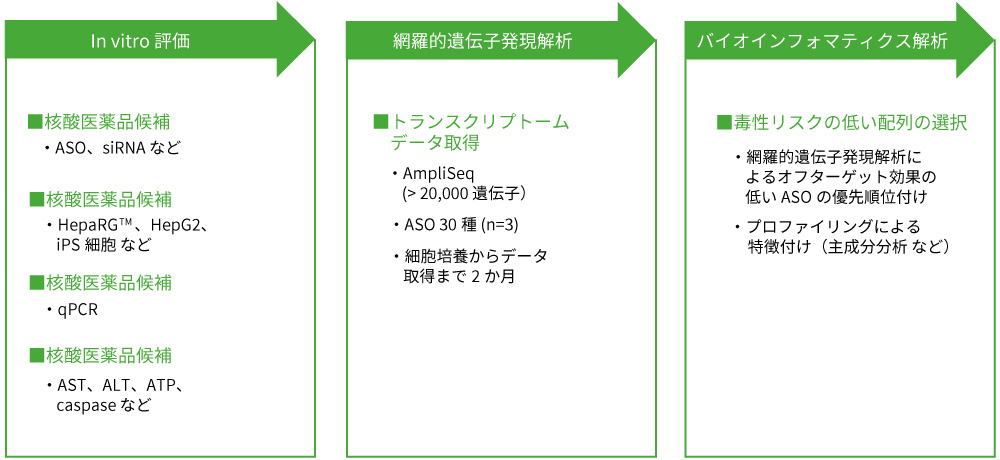
in vitro評価、網羅的遺伝子発現解析、
バイオインフォマティクス解析までワンストップで提供
- お客様の核酸医薬品候補をお預かりし、ヒト細胞株へのトランスフェクションの実施、ターゲットKD/細胞毒性の確認、およびAmpliSeqデータ取得まで、ハイスループットに実施します。
- 必要に応じて、種々のパラメータを指標にヒトでの安全性予測に外挿性のあるデータを取得します。
- トランスクリプトーム解析により、オフターゲット効果の低い配列を選択することができます。
ご希望の細胞を用いた核酸導入実験を実施します
- 実績が豊富なHepaRGTM細胞以外にも、お客様ご希望の細胞を用いた核酸導入実験を承ります。弊社で導入条件の検討や標的遺伝子発現の確認等、事前の検討から対応可能です。実績のある細胞:HepaRGTM、HepG2、hiPS由来分化細胞など
- HepaRGTM細胞の場合、自社で構築した網羅的遺伝子発現DBを活用することで、
評価対象遺伝子の発現の有無やその程度を事前に確認することが可能です。 - HepG2細胞の場合、384ウェルフォーマットのハイスループットな細胞毒性評価系(ATP、caspaseなど)との組み合わせにより、毒性の初期スクリーニングとオフターゲット効果(狭義)を同時に評価することが可能です。
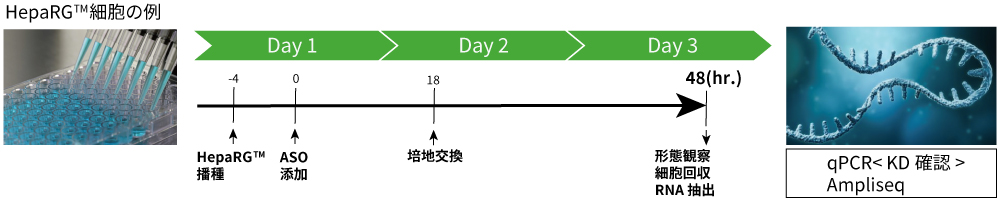
網羅的遺伝子発現解析による多面的アプローチ
- 網羅的な遺伝子発現解析によって、(1)標的遺伝子のノックダウン活性と(2)オフターゲット効果による遺伝子発現変動を同時に評価することができます。オフターゲット効果の低いASOの選択および優先順位付けが可能になります。(A)
- 主成分分析によって、網羅的な遺伝子発現データからASOのプロファイリングが可能になります。(B)
病理ピアレビューの実施により、
毒性試験の病理データの質と信頼性を向上
病理ピアレビューの実施が、OECDガイダンスによって推奨されています。その背景には、病理データがパソロジストの知識・経験・主観に左右される側面があり、経験豊かな第三者のパソロジストによるピアレビュー実施が望まれています。Axceleadには、創薬経験を持つ熟練のパソロジストが複数名在籍しており、毒性試験の病理ピアレビューを実施することで、病理データの質と信頼性を向上させます。
様々な毒性試験において、お客様の目的に合わせた病理ピアレビューを実施
- げっ歯類・イヌ・サル・ブタの毒性試験の病理検査について、GLP基準の公式ピアレビューあるいは簡略的な非公式ピアレビューなど、お客様の目的に合わせた病理ピアレビューを実施します。
- 病理ピアレビューの一環として、毒性試験の中で認められた所見の判断や解釈などのご相談をお受けいたします。
- 他施設で実施した毒性病理検査の病理ピアレビューを実施することが可能です。
- Whole slide imageを用いたテレパソロジー(webを活用した遠隔病理評価)による病理ピアレビューについても、ご要望に応じて検討いたします。
経験豊富なパソロジストが、セカンドオピニオンとして
公正かつ的確な病理ピアレビューを実施
- JSTP認定毒性病理学専門家、JCVP認定専門家である熟練のパソロジストが在籍しています。
- GLP及びINHAND(毒性病理用語・診断基準国際統一化)に精通した経験豊富なパソロジストが病理ピアレビューを実施することにより、所見の精度や信頼性を高めることができます。
- 第三者のパソロジストが客観的な視点で病理ピアレビューを実施することにより、病理データの納得性や信頼性が高まります。
- お客様の若手パソロジスト育成を目的とした教育的な病理ピアレビューも受けております。
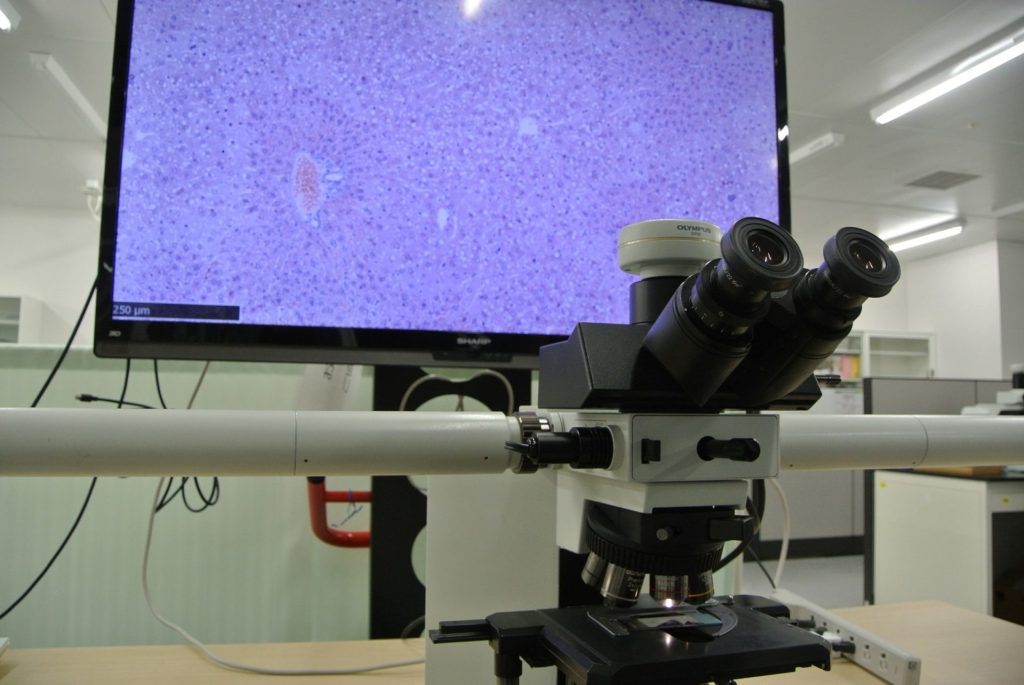
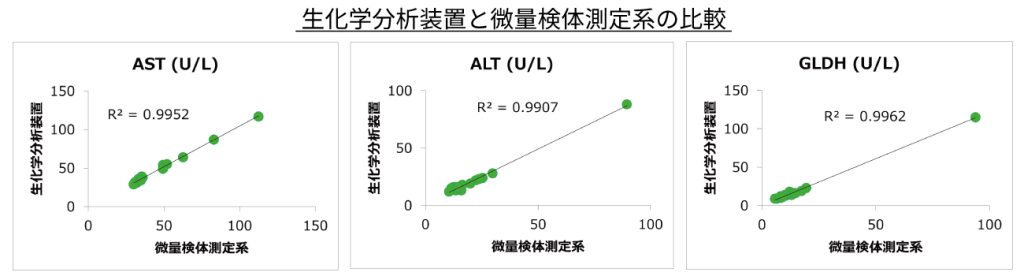
微量検体を活用し、創薬研究初期から肝・腎障害を評価
わずか20 μLの微量検体を最大活用!
- Axceleadは、創薬研究の初期段階から肝・腎障害を検討するために、これまで100 μL以上の検体量が必要であった血液生化学検査を改善しました。すなわち小動物の健康状態に影響が無い採血(頻回を含む)で得られる程度の微量血液で臓器障害マーカーを評価できるように、微量検体の肝・腎障害マーカー測定系を構築しました。
- 肝臓・腎臓は薬物の主要な代謝臓器であり、薬物による肝・腎障害の見極めは非常に重要です。開発初期段階から手持ちの血漿・血清を有効活用し、肝・腎障害の懸念を払拭しませんか?
- わずか20 μLで肝障害マーカー(AST, ALT, GLDH)1)または腎障害マーカー(Cre, UN)2)の評価が可能です(肝・腎障害マーカー両方で40 μL)。
- 別途、25 μLで臨床検体あるいは非臨床検体(サル、イヌ、ブタ、ラット、マウス)のサイトカインなど最大100項目の評価が可能です。
- P1・P2レベルの検体に対応できます。
- 限られた検体量の中で、お客様の課題解決に必要な測定項目をご提案します。
1) AST: Aspartate aminotransferase, ALT: Alanine aminotransferase, GLDH: Glutamate dehydrogenase
2) Cre: Creatinine, UN: Urea nitrogen.
創薬初期から肝障害を見極めることが重要です
- 臨床試験の中止や上市薬が市場から撤退する理由の多くは、薬物性肝障害(DILI)であり、全体の30%を占めます。また、近年開発が進む核酸医薬品には、肝臓や腎臓など特定の臓器に集積しやすい特徴があるため、それら臓器障害の有無を早期に見極めることは非常に重要です。
- DILIを見極めるために、肝障害バイオマーカーである肝逸脱酵素の血中AST・ALTが広く利用されていますが、AST・ALTは骨格筋にも多く発現していることが知られています。採血時の保定操作で骨格筋からAST・ALTが逸脱し、一見すると肝障害があるように見誤る可能性があります。Axceleadは、骨格筋の影響を受けない肝障害バイオマーカーとしてGLDHを採用し、AST・ALT・GLDHを測定する事で肝障害を的確にとらえます(第44-46回日本毒性学会にて、ラット、イヌ、サルにおける肝逸脱酵素(ALT, AST, GLDH)の臓器・組織分布及びその種間比較として発表)。
カニクイザルにおける肝逸脱酵素(ALT, AST, GLDH)の臓器・組織分布

お客様の課題解決に必要なサポートのご提案
- マルチプレックスアッセイは微量検体から沢山の情報を得る事ができ、多様なキットが販売されていますが、どれを選んだら良いかお悩みではないですか?
- GLP/Non-GLP毒性試験を長年担当してきた経験豊富な研究者が、お客様の課題解決に最適なキット・評価項目をご提案いたします。例えば、急性炎症の評価に用いられる急性相反応タンパクは、ヒトではCRPが用いられますが、げっ歯類ではCRPに比べSAA(Serum Amyloid A)の方が炎症に対して鋭敏に反応するため、げっ歯類の急性炎症の評価にはSAAをお勧めしています。このような種差の他、検体採取の条件などもご提案いたします。
- ICH3)-Q2分析法などガイドラインを準拠したバリデーションの実施も可能です。
3) ICH: International Council for Harmonisation of Technical …
統合トランスレーショナル研究 浅野研究員の共著論文が『Scientific Reports』に掲載されました!



Characterization and reduction of non-endocrine cells accompanying islet-like endocrine cells differentiated from human iPSC
2022年4月
https://www.nature.com/articles/s41598-022-08753-5
論文の概要:
糖尿病の根治的な治療法として、ES細胞やiPS細胞などのヒト多能性幹細胞から作製した膵島様細胞の移植が期待されています。人工的に細胞を作製すると目的外の細胞が混入する可能性があります。特に大量の細胞移植が必要となる臨床応用にむけて、安全性の観点から可能な限り混入を低減することが望まれますが、混入する細胞は非常に稀な細胞集団であるため、解析が困難で不明な点が多いという課題があります。
日吉秀行 主任研究員(武田薬品工業株式会社T-CiRAディスカバリー)、佐久間健介 主任研究員(前職:武田薬品工業株式会社T-CiRAディスカバリー、現職: オリヅルセラピューティクス株式会社)、山添則子 主任研究員(前職:武田薬品工業株式会社T-CiRAディスカバリー、現職: オリヅルセラピューティクス株式会社)および豊田太郎 講師(CiRA増殖分化機構研究部門、T-CiRA、現 未来生命科学開拓部門)らの研究グループは、 ヒトiPS細胞由来の膵島様細胞の遺伝子発現を単一細胞レベルで解析することで、製造過程で混入の可能性がある目的外細胞の特徴を同定し、高感度に検出する方法を見出しました。また、目的外細胞の除去方法として、細胞増殖に関わるPLK分子の阻害や、解糖系の阻害といった新規の方法が有効であることを示しました。これらの知見は、移植治療のためのヒトiPS細胞由来膵島様細胞の大量製造において、既存の方法と組み合わせて目的外細胞を除去し、安全性を高めることに役立つと期待されます。
本研究においてAxceleadはシングルセル遺伝子発現解析を担当しました。
シングルセル遺伝子発現解析
関連情報:

遺伝子改変マウス・ラット作製
ターゲット/バイオマーカー探索や病態を再現するために、
多様な遺伝子改変マウス・ラットを作製・繁殖し、
お客様の創薬課題を解決します
ターゲット/バイオマーカー探索や薬効薬理試験に、病態モデル動物は非常に有用です。Axceleadでは、ES細胞による相同組換え法やCRISPR/Cas9によるゲノム編集技術を用いて、短期間でユニークな遺伝子欠損(KO)、遺伝子ノックイン(KI)などの遺伝子改変マウス・ラットを作製いたします。作製した遺伝子改変マウス・ラットを用いて、表現型解析や薬理・病理評価までを一貫した体制で受託することができるため、より短期間で試験結果をご提供いたします。
次のようなご要望がありましたら、ぜひ我々にご相談ください。
核酸医薬品評価のために長鎖DNA配列をKIしたい
関連性の高い複数の遺伝子を一度にKOしたい
既存の病態モデルに遺伝子改変を行いたい
短期間で多くの遺伝子改変動物を解析に使いたい
モデル作出から解析までのトータルソリューション
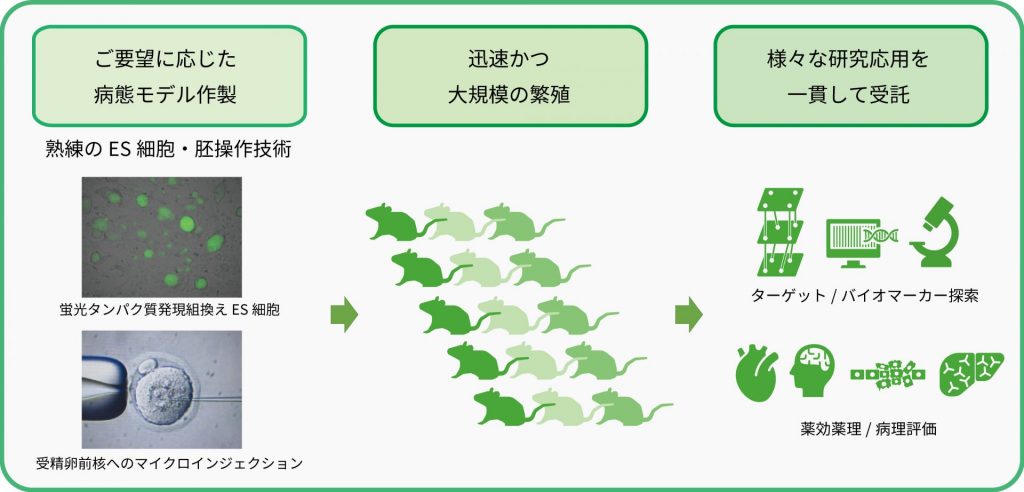
AXCCマウスを用いた腎疾患(CKD)創薬/病態研究
Mc4r KOマウスを用いたNASH治療薬/病態研究
ヒト型のエクソン・イントロン構造を保持したマウス
‐40kbpまでの長鎖KIが可能‐
近年、核酸医薬品を中心として、ヒトのゲノムDNA配列をターゲットとした薬剤の研究開発が活発となり、エクソン・イントロン構造を保持したヒト型KIマウス・ラットの需要が高まっています。 Axceleadでは、ES細胞やゲノム編集技術を用いてヒト型の長鎖KIマウス・ラットを作製いたします。これにより、ヒト型配列での薬剤の挙動や効果を生体で解析することができます。ご要望に応じて、核酸創薬研究をお手伝いするサポート体制を整えております。
ES細胞を用いた相同組換え法では、最大40kbpのKIマウスを取得
ゲノム編集技術を用いた手法では、最大17kbpのKIマウスを取得
KIラットの作製も可能

多層オミックス解析による
臨床応用可能なバイオマーカー探索
- ノンターゲットプロテオーム解析による蛋白質の網羅的な比較定量分析が可能です
- 蛋白質のリン酸化やユビキチン化など、翻訳後修飾に特化したプロテオーム解析が可能です
- 疾患特異的なアミノ酸配列を同定するためのデータベースを保有しています
- 安定同位体ラベル化アミノ酸を用いた蛋白質のターンオーバー解析が可能です
- 医薬品候補の治療効果を予測できる指標を見つけたい
- 医薬品候補の作用メカニズムを解明したい
- 医薬品候補に効果がある群(レスポンダー)を特定したい
- Axceleadでは、ヒト検体を用いたオミックス解析の実績があります
- 多群・多検体の生体試料の取り扱い及び分析・解析が可能です
- トランスクリプトーム、プロテオーム、メタボロームの各層のオミックスデータを取得できます
- バイオインフォマティクスによって多層オミックスデータの解析及び解釈が可能です
- ノンターゲットプロテオーム解析による蛋白質の網羅的な比較定量分析が可能です
- 蛋白質のリン酸化やユビキチン化など、翻訳後修飾に特化したプロテオーム解析が可能です
- 疾患特異的なアミノ酸配列を同定するためのデータベースを保有しています
- 安定同位体ラベル化アミノ酸を用いた蛋白質のターンオーバー解析が可能です
このような課題はありませんか?
Axceleadは、疾患モデルの作成、多層オミックス解析、PK/PD解析などのソリューションによってこれらの課題を解決することで、医薬品開発の成功確率向上を支援します。
オミックス解析は、生体内の状態を分子レベルで網羅的に定量化することにより、生体メカニズムを解明することができる手法です。Axceleadは、トランスクリプトミクス、プロテオミクス、メタボロミクス、リピドミクスなどのオミックス解析を実施するプラットフォームを有しており、バイオマーカーの探索から検証まで、全てのプロセスを実施することが可能です。これまでの医薬品開発の経験をもとに、試験デザイン、オミックスデータの解釈、仮説構築をサポートします

あらゆる生体試料の多群・多検体・多層オミックス解析が可能です

プロテオーム解析プラットフォーム
「Axceleadに聞いてみた」シリーズ:
創薬の成功を左右する「創薬標的のバリデーションのエキスパートに聞いてみた
日時:
2021年12月16日(木)12:00 – 12:30
概要:
創薬研究における創薬標的のバリデーションは、プロジェクトの進め方や価値、および創薬の成功率に大きな影響を与える重要なディシジョンポイントです。
バリデーションには、ツール(標的細胞、阻害薬など)が重要ですが、Axceleadでは、ツール化合物をはじめ多くのバリデーションに欠かせないツールが充実しており、さらにはこれらを駆使した蓄積されたノウハウがあり、創薬研究に重要な創薬標的探索のソリューションを提供しています。
今回は、製薬企業での豊富な創薬研究経験を持つ2人のエキスパートが、創薬標的のバリデーションの課題に挑みます。
※本イベントは、視聴者の皆様から事前募集した創薬研究に関する質問に回答する形で進めさせていただきます。是非、皆様のご意見をお聞かせください。
募集内容
創薬標的のバリデーションにおいて解決すべき課題を幅広く募集いたします。
課題のレベルは問いません。どの領域の方からのご質問も幅広く受け付けます。
演者紹介:

戎野 幸彦 統合トランスレーショナル研究 シニアダイレクター
2005年大阪大学大学院医学系研究科博士課程修了後、Oklahoma Medical Research Foundationに留学。 関西医科大学、武田薬品工業株式会社、大塚製薬株式会社を経て、2020年9月より現職。
Axceleadの
空間的トランスクリプトミクス(Visium)サービス
– 診たい組織サンプルはありませんか? –

Visium HDについても受託サービスご提供を開始しております。ぜひお問合せ下さい 。
こんなお客様に
- 空間的トランスクリプトミクスを研究に取り入れたいが導入でお困りの場合
- 密なディスカッションや手厚いサポートをご要望の場合
- 臨床検体の解析を目的とする場合
空間的トランスクリプトミクスとは?
病理組織切片をサンプルとして網羅的な遺伝子発現情報を得ることで、組織や細胞の位置/形態情報を伴った遺伝子発現データを可視化し、様々な観点から解析できる技術です。Axceleadでは10x Genomics社のVisiumキットを用いてサービスをご提供致します。解析に用いるサンプルはヒト及びマウス*の未固定新鮮凍結あるいはFFPEブロックが利用可能です。Visium解析の活用場面はトランスレーショナル研究、ターゲット探索/検証、MOA解析、病態解明など様々です。
バイオマーカー探索への活用
*場合によってはその他の動物種も解析可能ですのでご相談下さい
Axceleadの強み
Visium解析に必要となる病理ならびにバイオインフォマティクスを中心とした知識技術と、その連携による提案力です。お客様の様々なご相談に対し、蓄積してきた経験と実績を活かしながら試験デザイン、研究立案の部分も含めたご提案をさせて頂いております。弊社サービスの特長上、困難な課題が持ち込まれることが多いですが、解決に導くためお客様と密に連携しながら研究を進めます。
お客様の声をぜひご覧ください。
体細胞変異カスタムパネル解析
すべてお任せください!疾患に関連する
体細胞変異を検出する高効率ソリューション
腫瘍細胞における体細胞変異のプロファイルは、発症メカニズムを明らかにし薬剤の有効性や安全性を高めるために重要な情報となっています。Axceleadにご依頼いただければターゲット領域を特異的に増幅したNGS解析を実施することで、ごく少量のゲノムDNAから多検体の体細胞変異を効率よく検出することが可能です。
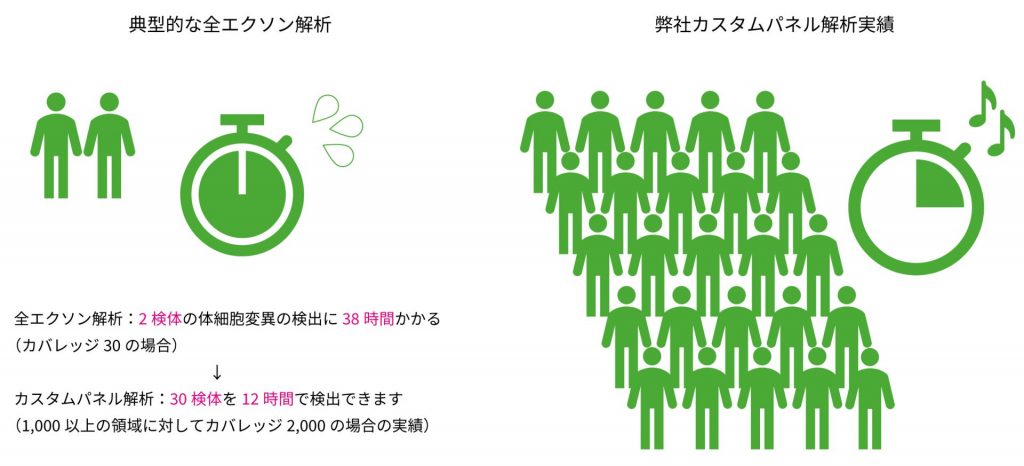
わずか10ngのゲノムDNAから、疾患に関与する
1,000を超えるサイトの変異を同時検出が可能
弊社のカスタムパネル解析をご利用いただければ、多検体の体細胞変異を効率よく検出することが可能です。全エキソン解析(WES)などノンバイアスに体細胞変異を検出する方法は探索的な研究では有効ですが、膨大なノイズを含む出力から疾患に関連する変異を見出すことは決して容易ではありません。また、解析するゲノムの範囲が膨大になるため、少ないカバレッジであってもトータルのリード数が多く必要となり費用面で高額になります。
疾患パスウェイに関連するゲノム領域に最初から絞ることにより、効率の良いデータ取得・解釈が可能となります。また、弊社のカスタムパネル解析では、PCRを用いて増幅するため、少量のゲノムDNAからでも解析することができます。
Axceleadでカスタムパネルのデザインからデータ解析まで対応可能
お客様から頂いた試験計画を元にカスタムパネルのデザインから、データ解析までワンストップで対応可能です。是非ご相談ください。
安全性の課題に対するソリューション
1. 網羅的な遺伝子発現解析によるオフターゲット毒性 (狭義) の評価
ヒトでのオフターゲット毒性リスクの低い配列を選択するため、ヒト細胞株を用いた網羅的な遺伝子発現解析を行います。
オフターゲット遺伝子が認められた場合、当該遺伝子の毒性情報調査を行いリスク評価をサポートいたします。
臨床での安全性情報が知られている核酸医薬品を参考データとして、お客様の核酸医薬品候補の遺伝子発現データを解析することで、
ヒトでの毒性リスクの低い候補品の選択に貢献します。
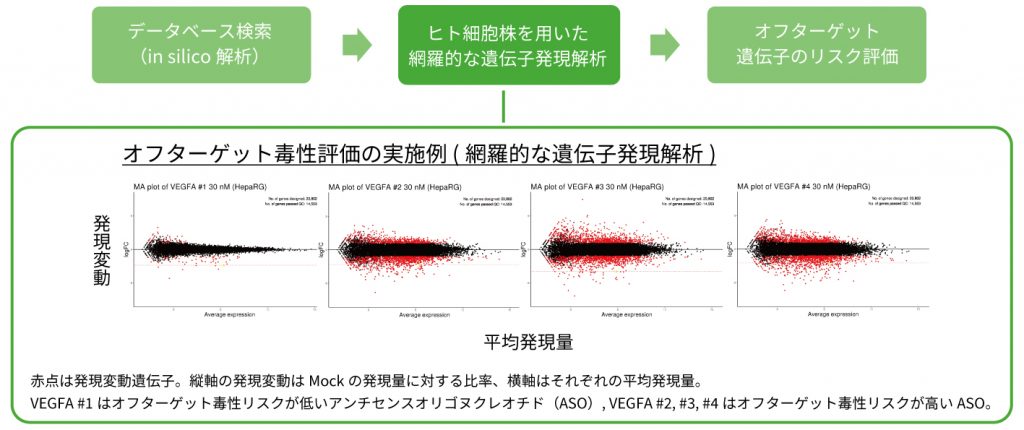
【臨床での安全性情報が知られているASOのオフターゲット毒性評価実例】
日本核酸医薬学会第6回年会にて発表
『Evaluation of the extrapolation about the off-target effects of antisense oligonucleotides from in vitro to human』
2. 多様な毒性評価系によるオフターゲット毒性 (広義) の評価
核酸創薬で注意すべき血液系・免疫系への影響や肝・腎毒性等を評価することにより、毒性リスクの低い核酸医薬品候補を選択します。
Axceleadではこれまでの豊富な創薬経験を活かし、各種毒性プロファイルについて、どのタイミングで・どの種類の毒性試験を実施すべきか、戦略面からご提案します。
また、in vitro・in vivo試験共に、下記のような多様な評価系を有しておりますが、お客様とご相談しながら、目的に応じたオリジナルな評価系も構築いたします。
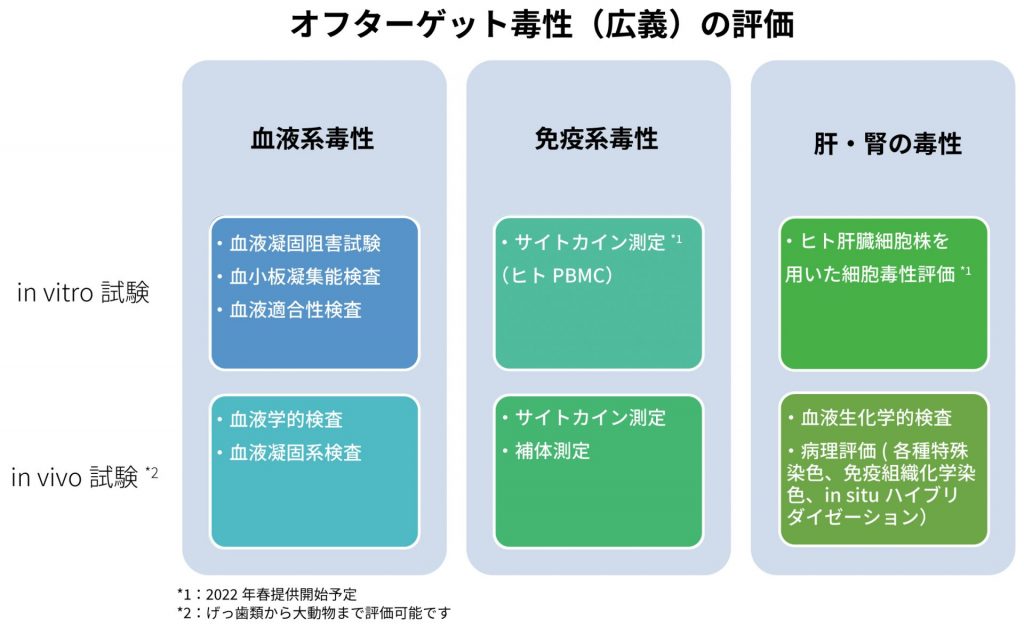
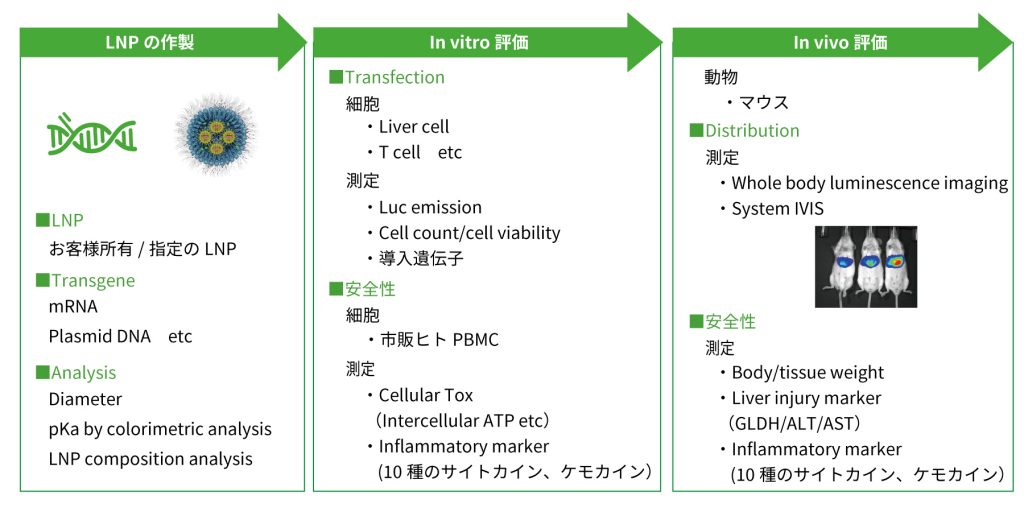
3.LNPの作製および免疫刺激性評価
Axceleadでは、遺伝子導入(mRNA, siRNA, DNA etc)のための Lipid nano particle (LNP)を用いた評価をサポートいたします。
標的組織・細胞への送達の課題に対するソリューション
細胞内動態評価 細胞内動態評価 細胞内動態評価 血漿/臓器中濃度評価 保有機器(LC/MS) 細胞内動態評価 薬効が不十分な場合に、標的組織の細胞までの送達が十分でないことが原因の一つとして考えられます。 血漿/臓器中濃度評価 保有機器(LC/MS) 細胞内動態評価
最新の機器を用いて迅速に血漿中、臓器中濃度を評価
・ Orbitrap Exploris 120
(ThermoScientific) 
1. 標的組織の細胞までの送達評価 (PK/PD解析)
Axceleadでは、様々な手法を組み合わせて動態上の課題を解析し、ボトルネックとなる工程を見出します。
まず、得られた動態結果 (PK解析)とPD解析結果から、送達が十分か否かを考察します。更に、薬理試験における投与レジュメのご提案も可能です。
病態モデル動物を用いた薬効評価
最新の機器を用いて迅速に血漿中、臓器中濃度を評価
・ Orbitrap Exploris 120
(ThermoScientific) 
ICHガイドライン未整備の課題に対するソリューション
最適なGLP試験パッケージのご提案
探索段階のデータを基に書面評価を実施し、お客様の目的(IND申請等)に応じた毒性試験GLPパッケージをご提案いたします。100品目以上のIND等の経験を有する専門家が、試験全体のマネジメントに加え、安全域の解釈や毒性課題の解決までサポートいたします。
非臨床安全性評価をトータルサポート
例えばこのようなシーンでご用命ください!



薬効評価の課題に対するソリューション

【弊社における病態モデル動物を用いた薬効評価の実例】
「非アルコール性脂肪肝炎の病態モデルマウスを用いたACC阻害薬の薬効評価」
・病因:生活習慣病
・病態:脂肪肝や肝線維化
・病態モデル動物:高脂肪食を負荷させたMC4受容体欠損マウス
・PD:肝臓中マロニルCoA
・薬効:脂肪肝や肝線維化の抑制
MC4R KOマウスを用いた薬効評価に関する論文 (PLOS ONE サイトへ)

1. ヒト細胞 (病態モデル)を用いた多様な表現型解析
各種 Cell line やhiPS細胞由来分化細胞を用いた様々なヒト細胞 (病態モデル)を準備して、多様な表現型解析を行い、お客様の核酸医薬品候補の選択に貢献します。
経験したスクリーニングや化合物評価技術を応用することで、お客様とご相談しながら、目的に応じたオリジナルな細胞評価系も構築いたします。
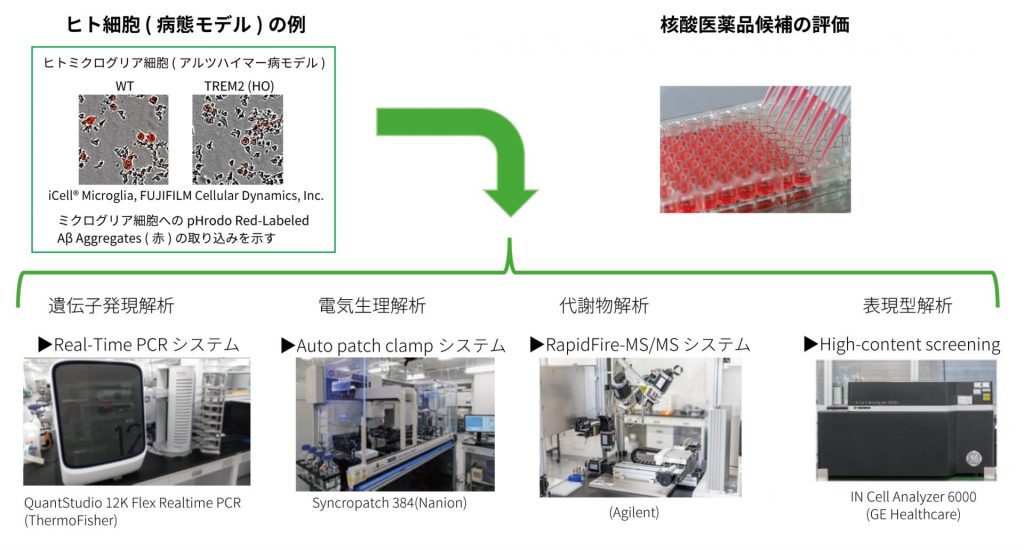
2. 病態モデル動物を用いた薬効評価
臨床外挿性の高い病態モデル動物において医薬品候補の薬効評価 (PD/薬効)を行い、臨床試験に向けたデータをご提供いたします。
お客様とご相談しながら、これまでの豊富な創薬の経験を活かして、必要最小限の試験デザインのご提案から薬効評価の実施まで対応いたします。
【弊社における病態モデル動物を用いた薬効評価の実例】
「非アルコール性脂肪肝炎の病態モデルマウスを用いたACC阻害薬の薬効評価」
・病因:生活習慣病
・病態:脂肪肝や肝線維化
・病態モデル動物:高脂肪食を負荷させたMC4受容体欠損マウス
・PD:肝臓中マロニルCoA
・薬効:脂肪肝や肝線維化の抑制
MC4R KOマウスを用いた薬効評価に関する論文 (PLOS ONE サイトへ)

Visium Dayにご参加の皆様
私たちは創薬ソリューションプロバイダーAxceleadです
“Partnership Research Organization(PRO)”として、
お客様と共に歩み、共に考え、日本から世界へ創薬イノベーションの創出を目指します。
Axceleadは、2017年に武田薬品工業株式会社の創薬プラットフォームを継承して事業を開始した、日本発の創薬ソリューションプロバイダーです。
製薬企業で長年培った豊富な技術や知識、経験を基に医薬品探索研究から臨床開発への橋渡しプロセスまで、お客様のニーズに合わせたソリューションを提供しています。
◆Axceleadのご紹介
約4分半でAxceleadをご紹介いたします。
まずは、私たちが何者なのかをご確認ください。
Axceleadのサービス一例をご紹介します
◆空間的トランスクリプトミクスとは?
Axceleadで提供している「空間的トランスクリプトミクス」とは?
バイオインフォマティシャンの坂口が、概要をご紹介します。
Laser Microdissection法
組織/細胞レベルでの領域特異的な解析により、
生物学的作用の機序解明やターゲット/バイオマーカー探索研究の課題解決を可能にします
Laser Microdissection法(LMD)とは、凍結切片やFFPE(ホルマリン固定パラフィン包埋)切片を専用スライドに載せ、顕微鏡で組織の観察を行いながら解析領域を採取する技術です。網羅的な遺伝子・タンパク質発現解析と組み合わせることで、目的の領域に特異的な現象を捉えることが可能になります。Axceleadでは、病理やオミクス研究の知識技術・経験を活かした統合的なサービスをご提供しております。
- 病変部位、特定構造やその比較対象を、解析領域として適切に見極めて採取することで、従来アプローチできなかった創薬ターゲットやバイオマーカーの探索/検証が可能となります。
- 病理組織像や作用機序に基づいて領域を設定することで、解像度を上げた薬効作用、毒性発現機序検証を実施することができます。
- ドラッグリポジショニングを目的に、お客様が保管されているFFPEブロックを再解析してターゲット探索/同定を実施することが可能です。
- 複合的なサービスとして、シングルセル/核-RNAseqなど周辺技術を用いた解析や薬効薬理試験との同時実施の形でご提供することも可能です。
シングルセル遺伝子発現解析
シングル核遺伝子発現解析
様々なサンプルに対応可能!
- Axceleadでは腎臓、膵臓、肝臓、眼球、卵巣、精巣、大動脈、癌組織やスフェロイドなど、様々な臓器/組織を扱った実績がございます。また、従来RNA断片化などの悪影響が懸念されてきたFFPEブロックについても、良好な結果が得られております。
- 事前検討として、解析に用いる組織の病理組織評価やRNAの質・量の確認を行い、サンプルの選別を実施することが可能です。例えば、臨床検体を用いてLMDからトランスクリプトーム解析を行う場合には、ブロックに含まれる組織成分とRNAの質・量が不均一であることが解析を妨げる原因になります。事前検討を実施しその結果を活かすことで、お客様の課題が解決できる可能性が高まります。
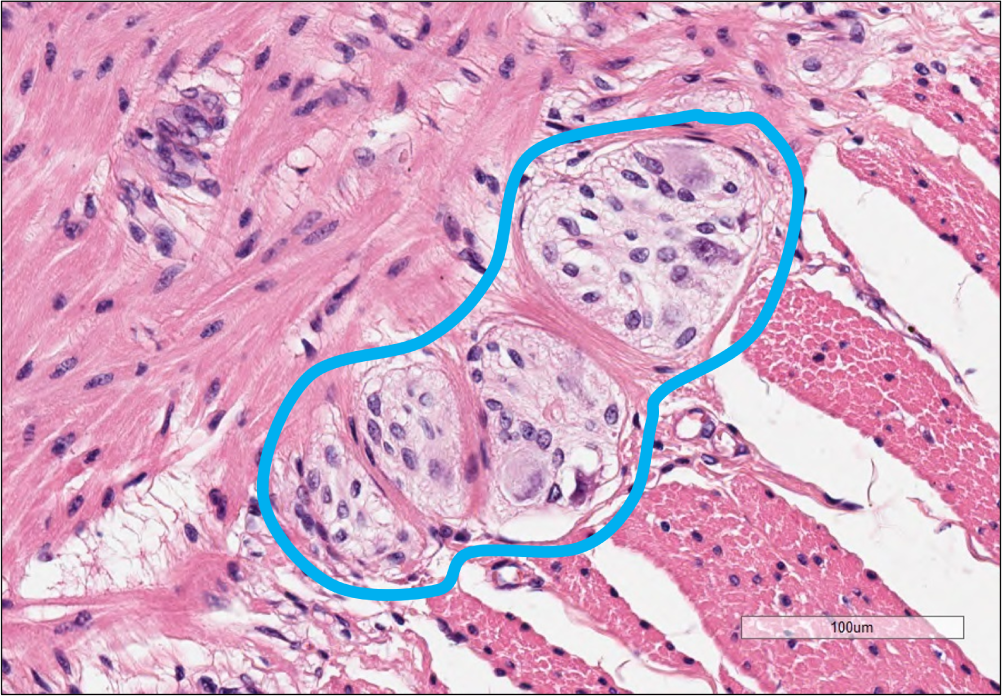
臨床検体で腸神経叢組織に着目した解析例。FFPEブロックを用いた解析例になります。
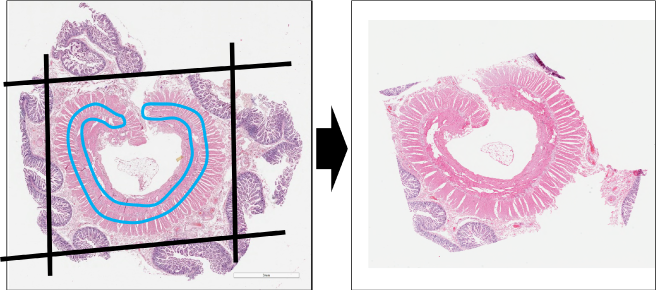
目的組織を含まない領域のブロックをトリミング除去して切片を作製することで、1枚のLMDスライドに載せる切片枚数を多くし、採取組織量を効率的に増加させることができます。
お客様の目的に合わせた適切な領域設定をご提案!
- 病理組織学的な観点からの病変/非病変部位の切り分けや、マーカー分子を利用した多重免疫染色による領域分類をご提案した実績がございます。お客様の目的に合わせた解析領域の設定をご提案させて頂きます。
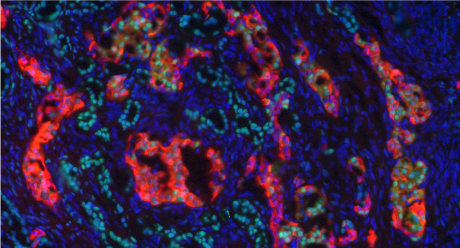
多重免疫染色の一例。マーカー分子を赤色蛍光(細胞質)と緑色蛍光(核)に染め分けることで、発現分子による領域分類が可能になりました。
遺伝子発現解析だけでなくタンパク質発現解析も可能!
- AxceleadではLMDとプロテオーム解析を組み合わせた課題解決の実績がございます。これまで解析が困難であるとされていた微量組織やFFPEでも対応可能なプロテオーム解析技術とセットでのサービスとしてもご利用下さい。
プロテオーム解析技術
フィンガープリンティング
フィンガープリンティングとは、化合物特有の遺伝子発現プロファイリングであり、Axceleadでは、化合物を用いたトランスクリプトームデータから、化合物に特異的なgene signatureを抽出し、フィンガープリンティングデータを作成します。
- Axceleadでは、AmpliSeqプラットフォームを有しており、少量のRNAから384プレートを用いたハイスループットのアッセイ系でトランスクリプトームデータを取得します。
- 化合物を用いたトランスクリプトームデータから、化合物に特異的なgene signatureを抽出します (フィンガープリンティング)。
- フィンガープリンティングデータを公共データベースと比較することにより、疾患候補の抽出(ドラッグリポジショニング)およびターゲット候補の抽出(ターゲットデコンボリューション)が可能になります。
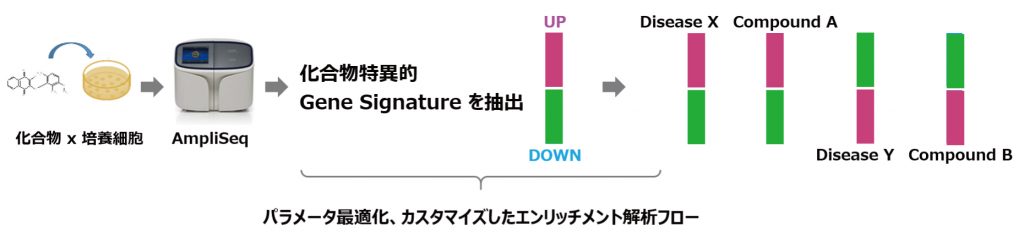
ターゲットデコンボリューション:
フェノティピックスクリーニング
ヒット化合物のターゲット同定!
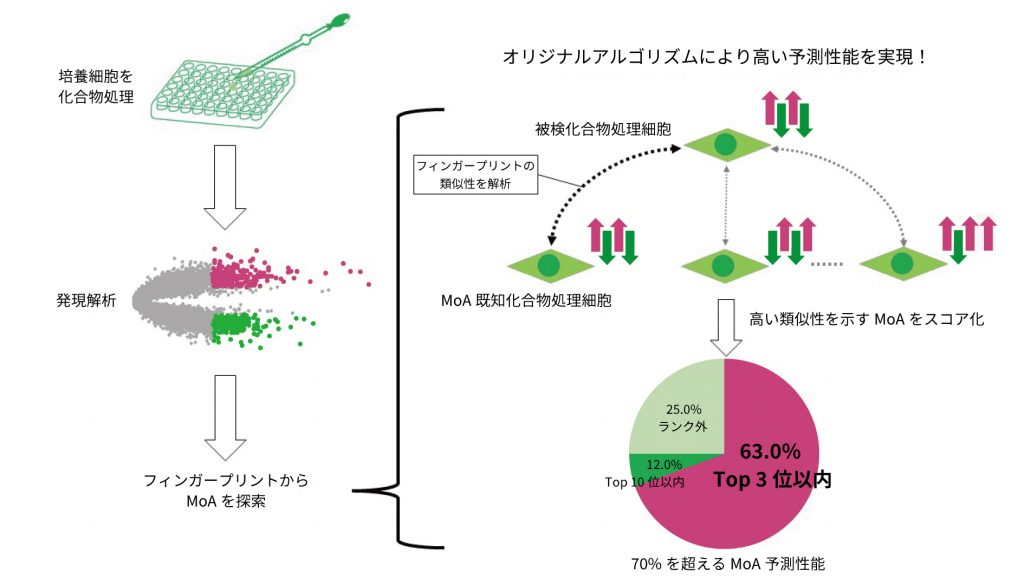
フェノティピックスクリーニングは細胞の表現型変化を指標とした化合物探索であり、従来のターゲットベースの化合物探索ではヒットしない化合物を見出す可能性がございます。同時に、ヒット化合物には作用メカニズムが不明な化合物が含まれる場合がございます。ヒット化合物を用いた創薬研究を進める上で、ヒット化合物の標的ターゲットの同定は解決するべき課題となります。我々は、ヒット化合物の標的ターゲットの同定を行うために、化合物から得たトランスクリプトームデータのフィンガープリンティングを行っており、標的分子の同定をいたします。
- フェノティピックスクリーニングから見出した化合物を用いたトランスクリプトームデータを取得し、化合物特有のgene signatureを抽出します (フィンガープリンティング)。
- 化合物特異的なgene signatureを用いて、ターゲット分子やMoAを推定します。
- 化合物の標的ターゲットを明らかにすることにより、創薬研究を加速することが可能でございます。
Axceleadの遺伝子改変動物作出機能や薬理薬効試験の統合的なサービスを提供することで、標的ターゲットの評価が可能となります。
Axcelead独自のデータベースを組み合わせることにより、標的ターゲットの確度高い推定を行います。
ドラッグリポジショニング:
新規適応疾患を探索!
ドラッグリポジショニングはお客様の財産である化合物を最大限に生かす事が可能であり、近年注目されているアプローチの一つでございます。開発化合物のライフサイクルマネージメントの観点から、既存化合物の適用疾患を拡大するために、適応疾患リスト作成が可能でございます。また、お客様が何らかの理由で研究開発を中止した化合物に関して、適応の可能性がある新たな適応疾患リストを作成いたします。
- 化合物を用いたトランスクリプトームデータから化合物に特異的なgene signatureを抽出します (フィンガープリンティングデータ)。
- 標的ターゲット分子に対する公共トランスクリプトームデータからターゲット分子に特異的なgene signatureを抽出します 。
- 化合物あるいは標的ターゲット分子に特異的なgene signatureを用いて、新規適用疾患候補を抽出します。
- これまでに培った経験により、解析の偽陽性・ノイズを効果的に除くことができます。
- In vitro研究の知識・経験を活かした総合的なサービスを提供しており、スピーディーに結果をご提供することが可能でございます。
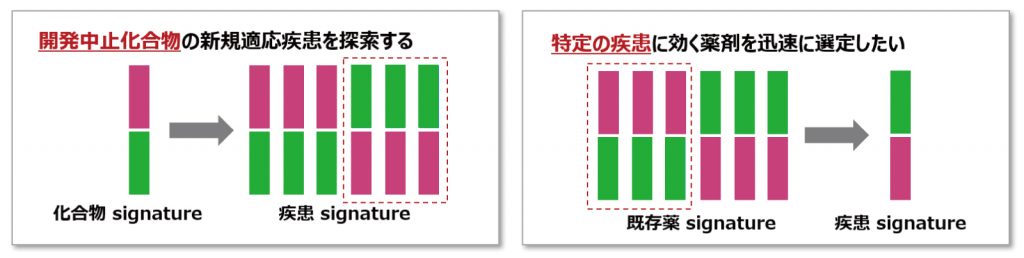
ドラッグリポジショニングのフロー。化合物に特異的なgene signatureと公共データベースとの比較解析により疾患候補を抽出します。
核酸医薬品の研究をサポートします!
日時:
2021年8月25日(水)12:00 – 12:30
概要:
核酸医薬品は、これまで低分子医薬品や抗体医薬品では標的とすることが難しかった遺伝性疾患等に対する新しいモダリティとして注目されており、近年世界的に研究開発が活発化しています。創薬ソリューションプロバイダーであるAxceleadでは、これまで培ってきた豊富な経験と技術力を活かし、核酸医薬品研究におけるソリューションを提供いたします。本セミナーでは、核酸医薬品の創薬研究における課題とその解決を中心に紹介いたします。
演者紹介:

吉田 唯真
統合トランスレーショナル研究 主任研究員
修士(環境科学)。日本環境変異原学会及び日本毒性学会会員。2013年静岡県立大学博士前期課程修了後、武田薬品工業入社。入社以来、主に候補化合物のin vitro毒性評価を担当し、2017年から核酸医薬品のin vitro安全性評価も担当。2017年7月よりAxcelead Drug Discovery Partners株式会社 非臨床安全性研究 in vitro毒性 研究員。2018年10月より現職。
マイクロダイアリシスで創薬研究にイノベーションを!
日時:
2021年8月3日(火)12:00 – 12:30
概要:
マイクロダイアリシス法は、創薬研究における強力なツールとなっています。
1970年代に開発されたマイクロダイアリシス法は、脳内の細胞外モノアミンなどの神経伝達物質を測定する方法として普及しました。現在では、中枢領域だけでなく、血液や末梢領域でも、さらには、病態関連ペプチドや、薬物濃度を測定するのためのツールとして幅広く使用されています。分析技術の発展により、複数種の同時測定や高感度分析が必要なバイオマーカーやセカンドメッセンジャーなどの変動をとらえることも可能となりました。
マイクロダイアリシス法と既存の評価系を組み合わせることで、創薬研究に新たな価値を見出すことができます。我々は、PK/PD/Efficacy 解析を活用して、ターゲット部位でのMOA 評価やPOM/POC 獲得にも応用しています。ここでは、マイクロダイアリシス法の実例や今後の展開についてご紹介します。
演者紹介:

前田 千恵
統合トランスレーショナル研究 統合生物 中枢疾患領域 主任研究員
薬学修士、薬剤師。大阪薬科大学卒業後、岡山大学大学院自然科学研究科医療薬学修士課程を修了。2003年に武田薬品工業に入社。睡眠リズム障害、認知症、精神疾患、神経変性疾患など、多岐にわたる中枢疾患領域の治療薬創製のため、数多くのプロジェクトに従事。
2017年 Axcelead Drug Discovery Partners株式会社設立時に武田薬品から転籍し、現職。3歳と11歳の2児の母。
パネルディスカッション:
進化するオープンイノベーション
~Unlock the value of Japanese Science~

協力:湘南アイパーク 後援:一般財団法人 バイオインダストリー協会
日時:
2021年9月8日(水)16:00 – 17:30
登壇企業:
オープンイノベーション(OI)を積極的に展開する企業と、ライフサイエンスエコシステム構築を目指す湘南アイパークからパネリストが登壇。

概要:
国内においても研究の効率化や外部の先端技術の活用を目的として、創薬研究にオープンイノベーション(OI)が活用されるようになって久しい。製薬企業はこぞって、ユニークな技術やシーズを持つアカデミアやバイオベンチャーとの連携を推進し、革新的な医薬品の創出を志してきた。一方、欧米は日本よりも大きく進んでいると言われており、強固な創薬エコシステムを背景に、特定の領域に特化した創薬ベンチャーが研究開発を進め、その成果を大手製薬会社が買収して世に出していくモデルが一般化している。
日本の創薬プレイヤーは、今後どのようにオープンイノベーションを展開していくべきか?今後も、日本から革新的な新薬を創出し続けるために、我々は今何に取り組めばいいのか?ライフサイエンスエコシステムの構築をミッションに掲げる湘南アイパーク。そのテナントの各業界代表者が本音をぶつけ合います。
パネリスト紹介:企業名アルファベット順
Meet a cutting-edge technology:
ドライーウエット融合型創薬を目指して
業務提携を行っているFRONTEOの豊柴氏をお招きし、開催いたします。
日時:
2021年7月15日(木)12:00 – 12:30
概要:
創薬においてもDX(デジタルトランスフォーメーション)の必要性が高まり、「IT創薬」、「AI創薬」が積極的に進められています。そこでは、ITやAI(ドライ)を通して仮説を構築し、実際に試験(ウエット)を行って構築された仮説を効率的に検証する、仮説・検証サイクルを効率的にまわすことが非常に重要です。本セミナーでは、FRONTEOの自然言語処理AIとAxceleadの創薬プラットフォームを組み合わせた、ドライーウエット融合型のリポジショニング・疾患探索の取り組みについて紹介します。
演者紹介:

豊柴 博義氏 株式会社FRONTEO ライフサイエンスAI事業部 CTO
博士(数学)早稲田大学大学院 理工学研究科数学専攻。理学博士(数学、2000年に博士号取得)課程中の1999年より九州大学医学部附属病院の医療情報部にて医療データの統計解析を担当する。2000年よりアメリカ国立環境健康科学研究所(NIEHS)において、データ解析による発がんプロセスの研究などに参加。2004年からは独立行政法人国立環境研究所にて、毒性データの統計解析・疫学研究のデザインとデータ解析の研究に従事。2006年に武田薬品工業に入社し、バイオインフォマティクス分野の研究員、グローバルデータサイエンス研究所・日本サイトバイオインフォマティクスヘッド、サイエンスフェローを歴任。また、臨床試験データにおける遺伝子発現データ解析やターゲット探索、さらに免疫と癌におけるバイオマーカー探索にも携わる。

「ペプチド創薬」が拓く中分子創薬
日時:
2021年7月21日(水)12:00 – 12:30
概要:
中分子創薬は、低分子薬と抗体の分子特性を併せ持つモダリティとして注目されており、その中で「ペプチド創薬」は、それぞれの利点を最大に活かすことができるアプローチとして期待が高まっています。本セミナーでは、Axcelead Drug Discovery Partnersが有するペプチド創薬のプラットホームや、ペプチド創薬の課題解決法について紹介を行います。
演者紹介:

医薬探索研究 主席研究員 寺尾嘉人
博士(工学)。2003年大阪大学大学院工学研究科博士後期課程修了。日本学術振興会特別研究員を経て、武田薬品工業株式会社に入社。創薬化学者として、新規化合物創出に従事。部門横断的な創薬プロジェクトをリード。2017年7月より現職。ペプチド、核酸、低分子を担当するMedicinal Chemistry&Modalityグループをリード。京都市出身
Meet a cutting-edge technology:
ヒト中枢移行評価を創薬初期段階から可能にする
Human BBB-on-a-chip
Axceleadが共同研究を進めている最先端技術をご紹介します。
日時:
2021年7月1日(木)12:00 – 12:30
概要:
ヒト由来細胞を用いた評価を、生体に近い環境で可能とする生体模倣デバイスMicrophysiological systemsは、外挿性の向上から近年非常に注目されている。BBB-on-a-chipは、中枢神経系を標的とした創薬において長年の課題である、探索段階でヒトにおける中枢移行を予測しうる評価系として期待される。本セミナーではiPS細胞とマイクロ流体デバイスによる三次元培養を駆使した最新の成果を紹介します。
演者紹介:

黒澤俊樹先生 帝京大学 薬学部 薬物動態学研究室 助教
博士 (薬学)。薬剤師。2020年に帝京大学大学院薬学研究科を修了後、同薬学部助教に就任。学部の頃から出口芳春教授のもとで血液脳関門 (BBB) 研究を開始し、薬物の脳移行に影響するBBBの複雑かつ巧妙なシステムに興味を持つ。大学院博士論文のタイトルは「ヒトiPS細胞由来脳毛細血管内皮細胞のBBBモデルとしての有用性」。現在はヒト脳微小環境を模倣する3次元培養モデルの開発に精力を注いでいる。第41回生体膜と薬物の相互作用シンポジウムで優秀発表賞を受賞。BBB関連の論文数は7報である。
「Axceleadに聞いてみた」シリーズ: 創薬の成功を左右する出発点「創薬標的探索」の エキスパートに聞いてみた
日時:
2021年6月24日(木)12:00 – 12:30
概要:
創薬研究における標的分子の選定は、その後の創薬の成功率に大きな影響を与える重要なディシジョンポイントです。
Axceleadでは、蓄積されたノウハウや、オミックス解析やバイオインフォマティクスなどの基盤技術を駆使してお客様のニーズに合わせた創薬標的探索のソリューションを提供しています。
今回は、製薬企業での豊富な創薬研究経験を持つ3人のエキスパートが、創薬標的探索上の課題に挑みます。
※本イベントは、視聴者の皆様から事前募集した創薬研究に関する質問に回答する形で進めさせていただきます。是非、皆様のご意見をお聞かせください。
募集内容
創薬標的探索フェーズにおいて解決すべき課題を幅広く募集いたします。
課題のレベルは問いません。どの領域の方からのご質問も幅広く受け付けます。
演者紹介:

医薬探索研究 主席研究員 尾野晃人
修士(工学)。大阪大学工学研究科修士課程修了後、武田薬品工業株式会社に入社。主に表現型スクリ―ニングを用いた医薬品探索研究に従事。2017年7月より、Axcelead Drug Discovery Partners株式会社分子スクリーニング主任研究員。2019年8月より現職。大阪府堺市出身
免疫抑制ブタを用いた薬効薬理試験
免疫抑制ブタを用いた薬効薬理試験ができます!
再生医療分野において、臨床外挿性の高い免疫抑制ブタを用いた薬効薬理試験が可能となりました。
お客様の臨床試験での成功確率向上に貢献いたします。
再生医療研究の分野では、ヒト細胞でつくられた再生臓器をヒトへ移植する前に、臨床と同じ手法での介入が可能な大型動物による有効性・安全性の検証が望まれています。一方、ヒトと大きさが近いブタにヒト細胞由来の再生臓器を移植した場合、異種移植によって生じる免疫応答の問題があり、本免疫不全ブタモデル開発以前は、ヒト細胞由来再生医療等製品のブタでの安全性・有効性の検証は困難と考えられていました。
Axcelead は、外科手術及び免疫抑制剤の薬物動態測定を基本とし、免疫抑制を個体毎のテーラーメードでコントロールした臨床外挿性が高い免疫抑制ブタを作製し、臨床試験の成功率を高めるようサポートをいたします。
免疫抑制ブタモデルの作製
- 外科的手術(胸腺及び脾臓摘出)および 免疫抑制剤の投与により免疫抑制状態にします。免疫抑制剤の投与用量は、ブタ末梢血単核球細胞を用いたin vitro 試験を基に設定し、投与後に目標血中濃度に達していることを確認します。
- 本モデルを用いて、異種移植やヒト細胞由来再生医療等製品の評価が可能となります。
- 病理評価による細胞生着、特異的な細胞マーカーを使用した細胞分化の程度を評価することができます。

病態モデルの作製例
◆ 免疫抑制心不全ブタモデル:
- 上記の免疫抑制ブタの左冠状動脈を結紮して、心不全を惹起するモデルを作製します。
- 3D エコーによる心機能評価ならびに細胞移植による有効性評価が実施可能です。
◆ 免疫抑制1型糖尿病ブタモデル:
- 上記の免疫抑ブタにストレプトゾトシンを処置し、1 型糖尿病モデルを作製します。
- 静脈内糖負荷試験などの評価ならびに細胞移植による有効性評価が実施可能です。
その他病態モデルの作製についてもご相談ください。

■ 免疫抑制ブタモデルの作製に関連する論文が「Nature research protocol Exchange」に公開されました
Axcelead の牧研究員、井垣研究員が共同執筆しています。
“Surgically produced, controllable immunocompromised pigs”
(Nature Research Protocol Exchange掲載情報)
Eiji Kobayashi et al., Posted …
シングル核遺伝子発現解析
凍結組織から1細胞レベルの
遺伝子発現解析ができる時代に
シングル核遺伝子発現解析(シングル核解析)は、1細胞から網羅的に遺伝子発現解析を行う手法であり、シングルセル遺伝子発現解析(シングルセル解析)では評価できなかった組織が対応可能な最先端の研究手法です。凍結組織を用いるシングル核解析により、従来のシングルセル解析でアプローチが困難であった疾患の病態機構解明が可能になります。Axcelead ではシングルセル解析に加えて、新たに難易度の高い脳組織の核取得技術を確立しました。さらに経験豊富なバイオインフォマティシャンが解析結果の考察までサポートすることで、遺伝子発現解析を基に新規創薬標的探索やバイオマーカー探索などの創薬研究を加速させます。
シングルセル解析では評価できなかった組織も対応可能に

シングル核解析が可能にすること
1.病態機構解明への新たなアプローチ
- 貴重な臨床検体の死後脳凍結組織を用いて、遺伝子レベル / 細胞レベルでの解析が可能になりました。
中枢領域のより深い生理機構 / 病態機構の理解をサポートします。
(例) レット症候群:Nature Neuroscience 2018; 21(12):1670–1679
アルツハイマー病:Nature 2019; 570(7761):332-337 - 細胞がダメージを受けやすい肝臓等も、凍結組織を用いることで、よ り正確な解析が可能になります。
(例)
シングルセル遺伝子発現解析
1細胞レベルでの網羅的な遺伝子発現情報を
よりスピーディーに高精度で解析できます!
次世代シーケンサーを用いたシングルセル解析では、iPS細胞の分化・未分化をより正確に評価することが可能になりました。更に、大量の遺伝子発現データをバイオインフォマティクス解析し、目的/非目的細胞のマーカーや、最適な分化誘導条件を導き出します。目的細胞を効率的に獲得し、お客様の再生医療研究を加速させます!
シングルセル解析で、より正確に評価
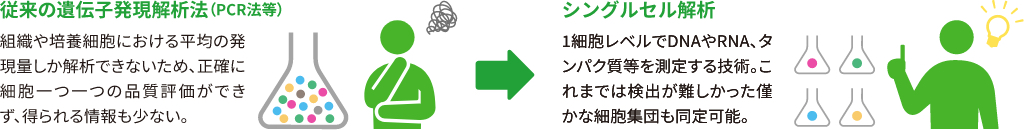
次世代シーケンサーで、よりスピーディーに解析
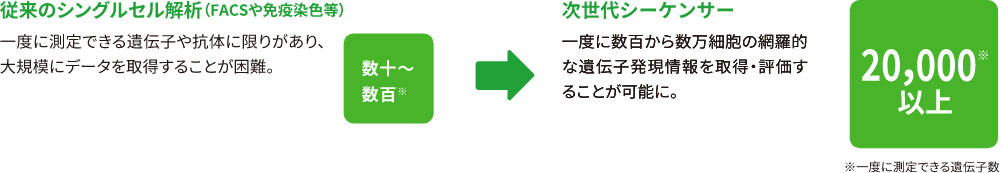
再生医療分野へのシングルセル解析の活用
1細胞レベルでの特性解析:
1細胞ごとの大規模な遺伝子発現データから、サンプル内の亜集団(サブポピュレーション)を検出し、サブポピュレーションごとに細胞種を推定します。これにより、目的細胞への分化の成否を正確に評価することが可能となります。
更に、見つかった目的/非目的細胞集団を判別できるバイオマーカーを探索し、効率的な細胞品質の評価をサポートします。
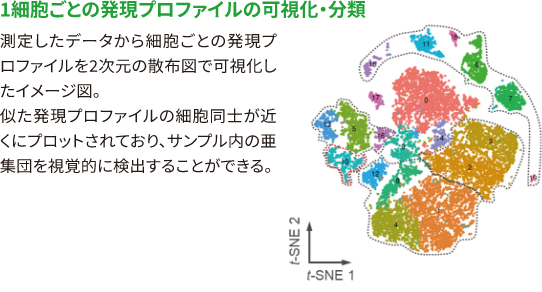
分化誘導の最適化
シングルセル解析で取得した細胞の擬似時間軸における発現変動を調べることで、細胞の分化経路や時系列における発現変動様式をとらえる事ができます。これらのデータから、細胞系譜の分岐に関わる遺伝子や、時系列に変動している転写因子を同定し、目的の細胞へ分化させるための最適な詳細条件をご提案いたします。
きれいな染色像では終わらない。
画像解析による定量データで薬効評価をサポート
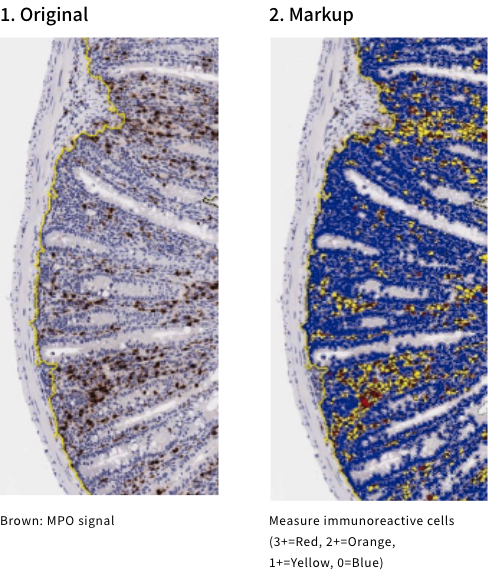
1. Original 投薬終了後のマウス腸管組織 サンプルに対して抗MPO抗体*を用いた免疫組織化学を実施。 * : 好中球のマーカー
2. Markup 免疫陽性反応(茶色)の染色強度を画像解析ソフトで数値化。
生体内の反応を最大限に評価する
AxceleadのIntegratedサービス
バイオロジーと安全性、一つ屋根の下にいる2つの部門が協力して、
無駄のない薬効評価試験デザインを提案します。
ワンストップで評価することで
スピーディで確かな考察を提供いたします。
【実施例】
大腸炎モデルマウスを用いた
薬理評価と炎症系細胞の画像解析
画像解析:

1. Original 投薬終了後のマウス腸管組織 サンプルに対して抗MPO抗体*を用いた免疫組織化学を実施。 * : 好中球のマーカー
2. Markup 免疫陽性反応(茶色)の染色強度を画像解析ソフトで数値化。
創薬研究におけるPK/PDの重要性 -PD評価系を駆使した研究ー
概要:
創薬研究において創薬標的に対してリード化合物の探索から最適化するプロセスを経て候補化合物を見出しているが、臨床試験まで進んだものは少ないのが現状です。このためトランスレーショナル研究が重要になっており、弊社においてはこの研究を進める上で重要であるPK/PD/薬効の観点から、臨床への橋渡しのサービスを展開している。今回、特にPD評価に着目してご紹介。さらにはバイオマーカー探索に関するサービスも合わせてご紹介します。
演者紹介:
修士(薬学)。1994年大阪大学薬学研究博士課程前期終了後、武田薬品工業に入社。創薬薬理部門において、アカデミアとの共同研究も含めて、骨・関節、炎症・免疫などの疾患領域での創薬研究の薬理を担当。免疫ユニット リサーチマネージャーを経て、2017年7月よりAxcelead Drug Discovery(株)統合生物 リサーチマネージャー、2020年4月から現職。武田薬品で培った知識・経験を生かして創薬研究をサポート。
臨床メタボロミクスによる層別化研究の実現に向けて
開催日時:
2021年3月18日 12:00〜12:30
概要:
創薬成功確率の向上のために、治療コンセプトが適している患者群の同定は重要です。この目的において、低侵襲的に採取可能なヒト体液を用いたオミックス解析は有用な手法と考えられています。一方で、臨床データは、被験者背景の多様性のため、大きな個人間変動を有することが知られており、その解決にはデータ数を増やすことが不可欠です。本セミナーでは、技術的に蓄積が困難と考えられていた臨床メタボロームデータの課題解決の可能性と、その応用例を紹介します。
演者紹介:

統合トランスレーショナル研究 主席研究員 安藤智広
2009年東京大学大学院薬学部研究科修了後、
武田薬品工業株式会社にて、薬物動態研究および、バイオマーカ研究に従事した。2017年より現職。
Integrated & Translational Science、Omics、主席研究員、薬学博士。
その他のセミナー
…
バイオインフォマティクスによる新たな価値創造:トランスクリプトーム解析を中心とした事例ご紹介
開催日時
2021年3月31日 12:00〜12:30
概要:
解析技術の進歩に伴い一つの実験で得られるデータ量は年々増大しています。Axceleadでは膨大で複雑な生物学データを解釈するために、種々のバイオインフォマティクス関連のサービスを提供し、お客様の課題を解決します。本セミナーでは、次世代シーケンサートランスクリプトーム解析(AmpliSeq 高感度アンプリコン解析、シングルセルRNA-seq)、公共データベースとの統合解析(エンリッチメント解析、パスウェイ解析)、MoA解析、ドラッグリポジショニングなど、多様なバイオインフォマティクス解析の事例を紹介します。
演者紹介:

統合トランスレーショナル研究 主席研究員 三井彰
博士(理学)。1986年大阪大学大学院理学研究科博士前期課程修了後、味の素株式会社に入社。分子生物学・遺伝子発現解析・バイオインフォマティクス技術を駆使して、創薬標的探索、薬剤作用メカニズム解析、バイオマーカー探索などの研究に従事。特に遺伝子発現解析は、PCR、マイクロアレイ、サンガーシーケンサー、次世代シーケンサーの黎明期から現在まで技術の進歩を間近に感じながら研究を行ってきた。1996年から2年間、米国MITに留学(Pillip Sharp研究室)。2020年8月から現職。バイオインフォマティクスをリード
その他のセミナー
「楽しい、面白い」はこれまでの自分の枠を越えるカギ
課題を解決してこそ答えがある
現在は、プラットフォームラボであるFrontier Technologyのオミックスチームで、LC/MS(液体クロマトグラフィー質量分析計)を用いた代謝物変動解析をしています。科学の道に進むことを志したきっかけは、中学生くらいの時とあるドラマを見て「病理医がかっこいい!」と思い、病理検査に従事する臨床検査技師を目指ざすようになったことと高校時代の生物の先生が面白い先生で。「問題を解いて答えがある」数学や生物がもともと好きだったこともあり、その先生のおかげでより生物が好きになっていきました。ただ、病理検査に携わることを目指していましたが顕微鏡をずっと覗いてるのは私の性に合っていなかったみたいで「自分には向いてないな」と感じていたとき、学校の先生に「生化学の方が向いてるんじゃない?」と言われて「確かに、生化学の方が好きだな」と感じたのに加え、判断基準がはっきりしていて「問題を解いて答えがある」のが好きな私には「こちらの方があってるかも」と思い、今の分析する仕事に至っています。
未知なる可能性へ
入社2年目の頃、初めてLC/MSに触れて私の理解の範囲を超えていて感動しました!サンプル量が少なくても測定できること。例えば、少ない採血量で患者さんにも負担が少なく測定することができるため、大きな可能性を感じました。触れる前は、名前は聞いたことがあるという程度で、どんな装置なのかあまりにもわからないことが多すぎました。ただ、LC/MSに可能性を感じたこともあり、どうしても使いこなせるようになりたくて、死に物狂いで調べまくりました!
とりあえずいろいろやってみよう!と思うようになったのは、この頃からだったのかもしれません。LC/MSという装置は、汚れが溜まると分析結果に影響が出てしまいます。「もっと知りたい!」と思いが湧いてきたことも加わり、今では自ら装置のメンテナンスをするようになりました!分解して洗浄することで「ここを洗えばこうなる」ということまで知ることができて面白いです。難事件を解決していく過程が面白くて小さいころから名探偵コナンが好きでした。探偵になりたいと思ったこともありましたがいまはこの仕事を通して解決していく過程を楽しんでいます。
性格を変えてくれたボードゲームとの出会い

プライベートでは、「カタンの開拓者」というボードゲームをよくやっています。もともとリアル脱出ゲームが好きで各地で開催されるゲームに参加していました。ある日、ゲームに参加されていた方と仲良くなり、「社会性身に付くからどう?」と誘われたのがきっかけです。
実際にやってみたら、どう交渉したら相手は動いてくれるんだろう?とか、同じボードゲームでもプレイする人が変わると全く違った展開になったりとその面白さにハマりました。「面白いからもっとやりたい!」「身近で一緒に出来る人が欲しい!」と思って社内で広めた結果、社長と一緒に遊んだこともあります!以前は、人見知りで恥ずかしがり屋だったので自分から何かに誰かを誘うことは滅多になかったんですがそんな自分を変えてくれた出会いとなりました。
心に響いた言葉を信じて
学生時代に「どんな名医がいても、生涯で助けられる人の数はそんなに多くないけれど、優秀な薬があればより多くの人を助けられる」という言葉聞いて以来、それを信じてここまでやってきました。今でもどんな形でもいいから創薬に携わりたいと考えています。
「自然はウソをつかない」語り掛ければ答えは返ってくる
多種多様な考え方と経験を掛け合わせ創薬と向き合う
現在は、統合生物・免疫疾患領域チームのリーダーとして、チームマネージメントの他、炎症・免疫疾患に関連する受託案件において試験遂行の管理や、薬理に関するコンサルテーション、創薬機能を跨る統合型創薬支援サービスにおける薬理部門のリーダー等を担当しています。大手製薬会社からアカデミア・ベンチャーなど、様々なクライアントが持つ多種多様な考え方や文化に触れ、新たなことを学び挑戦できることに面白さを感じています。自身の経験や考えを基に提案したアイデア、ソリューション案がクライアントに受け入れられ、試験を遂行できた時、また、その試験で良い結果が得られれば、更に嬉しく、楽しいです。
誰も知らないことを明らかにしていく面白さ
大学4年生の時、希望して入った研究室の教授に言われた「自然はウソをつかない」という言葉に衝撃をうけました!それまで考えたことがなかったことでしたし、その言葉を今でも大切にしています。自然はこちらから何かを問いかけるとアクションが必ず返ってきます。期待しない返事が返ってくるときは、違う問いかけをしてしまっているか、自身が立てた仮説が間違っているかです。いつも期待した答えが返ってくるわけではありませんが、やればやるだけ答えが返ってきます。新しい答えがわかると嬉しいですし、誰も知らないことを明らかにしていく面白さがあって研究にのめり込んでいきました。これが研究の楽しさだと感じています。
続けるヒケツは環境づくりから

プライベートでは、ランニングを10年ほど続けています。当時、私の周りで走り始めた方が数人いて、みんなで大会に出よう!ということになったのがきっかけです。その頃の仲間はみんなやめてしまったのと(笑)、生活の環境が変わってしばらく一人で走っていましたが、何だか寂しくなってしまい、ネットでランニングチームを見つけました。
現在は週1回、そのランニングチームでトレーニングに励んでいます。また、チームのメンバーは幅広い年齢層で、ほぼ全員が異業種で働く方々であり、走ること以外でもいい刺激になっています。
困難だからこそクライアントと共に叶えたい夢
製薬会社で研究者として働いていて、創薬の初期段階から携わった開発化合物が上市されるという幸運に辿りつけることは極まれであると言われながらも、新薬の創出を夢見て長年取り組んできました。Axceleadでは、多くのクライアントの皆様の創薬に関われることから、そのチャンスは格段に増えると思っています。引き続き、私とクライアントの共通の夢の実現、「革新的な新薬の創出」に向けて、日々業務に邁進していきます。
迷ったときこそ、困難な方へ
教科書に載るような写真を撮りたい!
2017年に武田薬品工業からAxcelead Drug Discovery Partnersへ転籍し血液検査や標本作製(免疫染色や画像解析なども)、そして病理組織検査を行うチームをリードしています。それぞれの技術を目当てに異なるお客様からご依頼を受けることもありますが、薬効試験や毒性試験といった場面ではひとつのチームであることを活かし、これらの技術を総合して動物の状態により深く迫れる(病態を理解する)ことに面白さを感じます。
そもそも、標本作製技術や顕微鏡観察技術に興味を持ったのは「教科書に載るような写真を撮りたい!」「模式図やイラストなど想像で描くのではなく、自分の目で見たことを載せたい!」と思ったからです。ですので、顕微鏡や染色方法など、組織を可視化するためのツールを使いこなせるようになりたくて、大学では専門の教授の元で学び、生物現象を可視化する方法を探求しました。
創薬に携わる自分の役割、取り組む姿勢の原点

社会人になって2年目のある日、今と同じように組織染色の仕事をしていたことがありました。薬の投与によってある神経細胞が活性化していることを示唆するきれいな写真が撮れ、定性的な結果として上司に報告したところ。「え、それで終わり?それじゃあ、Go/No-Goの判断できないじゃない。」と言われました。私は、組織染色に定量性を持たせることは不可能、無意味と考えていたため、そこで思考が停止していました。しかし、上司の一言で、会社の仕事とはそういうことかと気づかされ、すぐに、数十枚の画像について活性化している細胞の数をひたすら手動でカウントし続け、グラフに起こし、統計解析を行ったところ有意な変化として捉えることができました。その日は、ちょうど会社のレクリエーションがあり、外の庭でBBQが行われ、私も楽しみにしていたのですが、参加出来ずカウントは夜まで続きました。上司はBBQに参加はしたものの早々に引き上げて、居室に戻ってデスクワークを続け、深夜近かったのですが、私の報告が上がるまで静かに待っていてくれました。結果を報告すると、「よくやったね。ここまでやるのが会社の仕事。」と笑顔で言葉をかけてくれました。その日を境に、“染めるだけでは終わらない”、といった今の仕事への姿勢につながっています。
困難な方を選択したからこそ
武田薬品からAxceleadに転籍したことで、試験を委託する側から受託する側へ。一研究員として自身の研究・役割を遂行する立場から、チームをリードする立場へ。仕事内容も薬の種を作る仕事から、創薬研究の後期のフェーズである安全性へとガラッと変わりました。正直、お話をいただいた時は悩みました。責任も大きくなりますし、今までやったことのない仕事でしたから。ですが、これまでと同じ環境よりも困難に思える方を選択したのは、「迷ったときは困難な方を選択しよう!」と大切な人に言われたことがあって、以来、人生で何か悩んだ時や迷った時こそ困難な方を選択することを大切にしています。
結果、様々な価値観の方と出会うことが増えたことで、視野が広がり「これはこういうもの」という先入観が減り、以前と比べると柔軟性が高くなったように思いますし、その違いが面白いなと感じています。
立場が変わり見えたことを活かして
委託していた立場だったからこそお客様の気持ちを理解できることもあると思っています。しかし、お客様の気持ちにちゃんと寄り添えているか?といわれると正直、至らない点もあるかと思いますが、創薬に熱い想いを持った方に技術とアイデアで新たな視点を提供し、全力を尽くしてサポートさせていただきます。
創薬研究の未来を切り拓くオミックス解析
~多層オミックス解析によるメカニズム探索~
Axceleadでは、創薬研究に必要な先端プラットフォーム技術の拡充にも力を入れており、中でもこの10年で大きく研究の裾野が広がったオミックス解析についてご紹介します。創薬研究者ならではのこだわりや今後の展望など、新たな時代を感じるインタビューとなり、私も非常にワクワクしました!
大学の研究室からのキャリアチェンジ!
見えた世界・見たい世界
不安を抱えつつも可能性へダイブ!
今は統合トランスレーショナル研究 Frontier TechnologyシニアダイレクターとしてプラットフォームラボであるFrontier Technologyをリードしていますが、10年間、大学で研究をした後に、武田薬品工業に転職しました。企業へキャリアチェンジしようと思ったきっかけは、研究に没頭するだけではなく、より社会の役に立ちたい!自分の可能性を試したい!と思ったからです。でも、大学の研究室というある種特殊な世界でしか過ごしたことがなかったので、製薬企業での研究はどうなんだろう?外からみた武田薬品工業の印象はサイエンスのレベルが高そうでしたし、これまでやってきた研究や知識が通用するのか?ちゃんとやっていけるのかな?と正直不安でした。
実際に入社してみると、大学と企業では研究の目指す方向性が違っていました。自分の知的好奇心があるところを大学ではどんどん追及していくスタイル。製薬企業では決まった時間の中で成果を出さなければいけない。あとは、共通言語も違っていて、キャリアチェンジした時には周りの方に手伝っていただいて、独特な社内略語の一覧表をつくり覚えていました(笑)。慣れるまで半年~1年くらいかかりましたね。
チームで結果を出す楽しさ、多様性がもたらす化学変化
大学の研究室で働いていた時は、私が計画した研究を3人くらいのチームで行っていましたが、製薬企業では大きなプロジェクトになると、関わる研究者が100人くらいいて、「こんなに大きな仕事ができるんだ!」とダイナミックさに感動しました。大学の研究室だと関わる人が限られていましたが、企業にはいろいろな感性をもった方が大勢いて刺激的でした。バックグランドが異なる合成研究者と生物研究者がいる混合チームをリードしていた時に、多様性を力に変えて短期間で結果を出す楽しさと、専門の異なるメンバーで一つのことを成し遂げたよろこびを感じました。
「良い習慣は才能を越える」まず、やってみる。
もとから「まず、やってみよう!」というタイプではなかったのですが、大学からキャリアチェンジしたことで環境が変わっていろいろな感性に触れたり、ポジションが変わったことで求められるものが広がった結果、以前は書店で素通りするくらい手に取ることがなかったビジネス書を読んでいくことで考え方や感覚が変わってきたように思います。
特に変わったなと感じるのは会議での姿勢です。以前は会議で発言するのが苦手で、目立たないところに座って「話を振られませんように!」と思って過ごしていました。ある時から「最低1つは質問して会議に貢献しよう!」と決め、会議に積極的に参加するようにしてから、変わっていったと思います。質問するのも最初は勇気がいりましたが、自分を変えようと思って意識して習慣化することで、いつの間にか当たり前になりました。
プライベートではお酒と旅行が好きでしたが コロナ禍で外食や旅行が難しくなり、自宅で過ごす時間が増えたので、料理を始めてみました。ちょうどパンを焼く機械があったのでピザを生地から作ることに挑戦してみたのですが、ゼロから何かを作るという面白さにはまってしまい、今では得意料理のひとつです。仕事でもプライベートでも、「まず、やってみる!」ということを大切にしています。

ひとりひとりが楽しく
アカデミア、製薬企業、ソリューションプロバイダーとキャリアチェンジを重ねてきた私ですが、一貫して「創薬」に関わり続けてきました。病で苦しむ方に薬を届けたいという想いが原点にあったからです。それは父が医師であり幼いころから研究に触れていたからかもしれません。これまでに身に着けた自分の知識や経験を創薬研究に捧げることで、より多くの人々の健康に貢献したいと考えています。また、「画期的な医薬品の創出に貢献する」というミッションの元で働いているAxceleadのひとりひとりが笑って楽しく働ける環境であるように努めることも、私の使命だと考えています。