タンパク質分解誘導剤(TPD)創薬の総合ソリューション
Axceleadは、前臨床段階でのTPD創薬において、確かな実績と幅広い専門性を有しています。プロジェクトの部分的なサポートから全体の支援まで、研究者の皆様のニーズに合わせた最適なソリューションを提供します。
タンパク質分解誘導剤(TPD)の可能性
タンパク質分解誘導剤(TPD)は、創薬の分野で新たに注目される革新的な治療モダリティです。従来の治療法がタンパク質の機能を阻害するのに対し、TPDはユビキチン-プロテアソーム系などを活用して特定のタンパク質を分解します。これにより、疾患の原因となるタンパク質を選択的に除去することが可能になります。
タンパク質分解誘導剤(TPD)の特長と利点
- 幅広い適用範囲:従来は治療が困難だった標的(Undruggable Targets)への対応が可能
- 高い治療効果:疾患原因となるタンパク質を直接分解することで、深い治療効果を発揮
- 効率的な治療:触媒作用に基づき、必要な投与量を削減
- 安全性の向上:組織または細胞選択的な標的分解による副作用リスクの低減
- 非侵襲的な投与方法:経口投与が可能で、患者さんに優しい治療を実現
TPDの分類と課題
TPDは主に、PROTAC®のようなキメラ型分解剤と、モレキュラーグルー型分解剤に分類されます。キメラ型分解剤は、探索の初期段階で合理的に設計することが可能である一方、分子構造が複雑になるため、最適化・合成・精製・ADMEなどに課題があります。モレキュラーグルー型分解剤は、発見方法、選択性、分解メカニズムの同定などが課題になることがあります。
また、キメラ型分解剤・モレキュラーグルー型分解剤に共通して、高度に専門的かつ多様なアッセイ系が必要なことも課題となります。
Axceleadのプラットフォームがタンパク質分解誘導剤創薬の課題を解決
キメラ型分解剤
熟練のケミストがヒット化合物やリード化合物の創出、新薬候補化合物の探索を加速します。
- Axceleadの分解剤用化合物ツールボックス、多段階ハイスループット合成および精製技術を使用することで、これまでにない多様なケミカルスペースへの迅速なアクセスを可能にします。
- 有望なキメラ型分解剤をより確実かつ迅速に特定します。
- 複数の技術によって、最適な薬物動態特性を有するキメラ型分解剤を見出します。
- ドラッグデザインノウハウ
- キメラ型分解剤に適したADME評価技術
モレキュラーグルー型分解剤
- モレキュラーグルー型分解剤に特化したライブラリーにより、分解メカニズムを速やかに同定できるヒット化合物を見出す可能性が高まります。
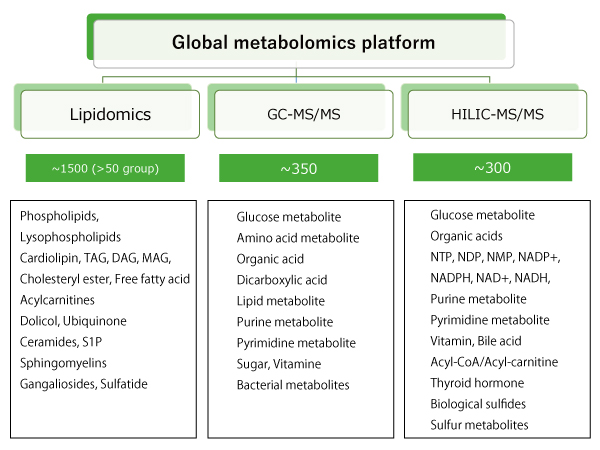
- グローバルプロテオミクスと近接ラベリング技術により、オフターゲットや新規ネオ基質の効率的な発見を支援します。
- 表現型スクリーニング後に、分解経路・メカニズムの同定(CRISPR-cas9、近接ラベリング、IPなど)を提供します。
- 多数のオリジナルのネオ基質候補を保有しており、お客様の興味のあるターゲットがその候補に含まれていれば、プロジェクトが加速する可能性があります。
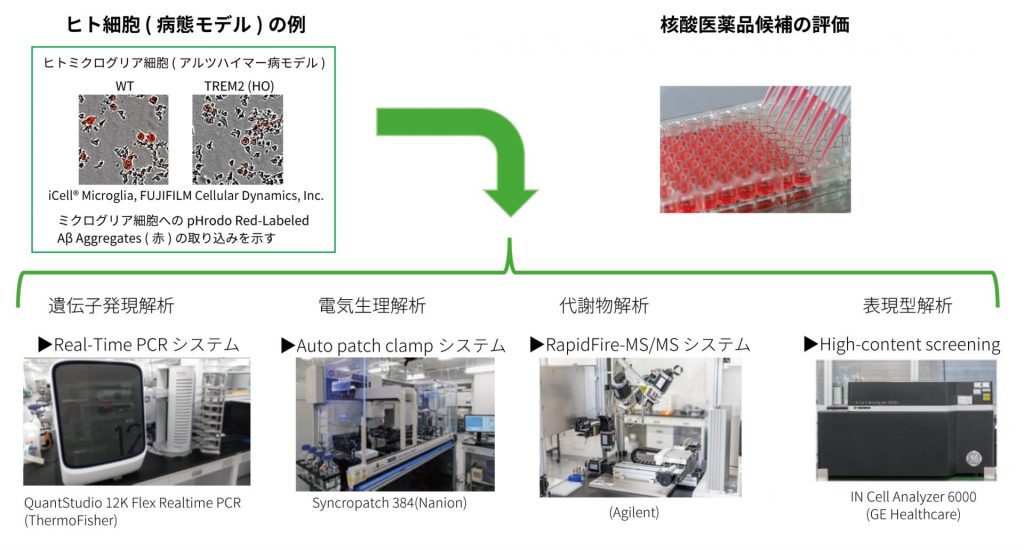
タンパク質分解誘導剤アッセイのケイパビリティ
専門性と多様性を備えたアッセイ能力
Axceleadは、以下のような最先端アッセイ技術を駆使し、TPD創薬を支援します:
- ハイスループットスクリーニング:HiBiT®、NanoBRET®、TR-FRET、Cell imaging、AlphaScreen
- 評価とプロファイリング:分解経路解析、プロテオミクス、E3リガーゼのスクリーニング、X線結晶構造解析
これらの技術と専門性により、研究者の皆様のプロジェクトを次の成功へと導きます。